
����Ŀ�����������ƣ�Na2S2O5����ҽҩ����ӡȾ��ʳƷ�ȷ���Ӧ�ù㷺���ش��������⣺
��1������Na2S2O5��ͨ������NaHSO3��������Һ���ᾧ��ˮ�Ƶá�д���ù��̵Ļ�ѧ����ʽ__________��
��2�������̵����е�SO2����Na2S2O5�Ĺ���Ϊ��

��pH=4.1ʱ������Ϊ__________��Һ��д��ѧʽ����
�������м���Na2CO3���塢���ٴγ���SO2��Ŀ����__________��
��3���Ʊ�Na2S2O5Ҳ�ɲ�������Ĥ��⼼����װ����ͼ��ʾ������SO2������Һ�к���NaHSO3��Na2SO3�������ĵ缫��ӦʽΪ_____________������__________�ҵ�NaHSO3Ũ�����ӡ���������Һ���нᾧ��ˮ���ɵõ�Na2S2O5��

��4��Na2S2O5������ʳƷ�Ŀ����������ڲⶨij���Ѿ���Na2S2O5������ʱ��ȡ50.00 mL���Ѿ���Ʒ����0.01000 mol��L1�ĵ��Һ�ζ����յ㣬����10.00 mL���ζ���Ӧ�����ӷ���ʽΪ_____________������Ʒ��Na2S2O5�IJ�����Ϊ____________g��L1����SO2�ƣ���
���𰸡� 2NaHSO3��Na2S2O5+H2O NaHSO3 �õ�NaHSO3��������Һ 2H2O��4e����4H��+O2�� a S2O52��+2I2+3H2O��2SO42��+4I��+6H�� 0.128
����������������1������ԭ���غ���д����ʽ��
��2���ٸ�����Һ�������жϲ��
��Ҫ�Ʊ����������ƣ���Ҫ�Ʊ����������ƹ�������Һ���ݴ��жϣ�
��3�����������������ŵ磬���������ӷŵ磬��������ӽ���Ĥ�����ý��
��4�������������뵥�ʵⷢ��������ԭ��Ӧ���ݴ���д����ʽ�����ݷ���ʽ�����������
��⣺��1�����������ƹ�������Һ��ˮ���ɽ��������ƣ�����ԭ���غ��֪��Ӧ�ķ���ʽΪ2NaHSO3��Na2S2O5+H2O��
��2����̼���Ʊ�����Һ����SO2�����Һ�����ԣ�˵������������ʽ�Σ�������ΪNaHSO3��
��Ҫ�Ʊ����������ƣ���Ҫ�Ʊ����������ƹ�������Һ����˹����м���̼���ƹ��塢���ٴγ�����������Ŀ���ǵõ�NaHSO3��������Һ��
��3����������ʧȥ���ӵ�������Ӧ����������ϡ���ᣬ�������ŵ磬��缫��ӦʽΪ2H2O��4e����4H��+O2��������������������ͨ�������ӽ���Ĥ����a�����������ƽ�������������ơ������������ӷŵ磬������Ũ�����������������Ʒ�Ӧ�����������ƣ����Ե���a�������������Ƶ�Ũ������
��4�����ʵ���������ԣ��ܰѽ�������������Ϊ�����ƣ���Ӧ�ķ���ʽΪS2O52��+2I2+3H2O��2SO42��+4I��+6H�������ĵ�����ʵ�����0.0001mol�����Խ��������ƵIJ���������SO2�ƣ���![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ�ػ��ϼ���ԭ�������Ĺ�ϵͼ������˵������ȷ����

A. ��̬�⻯����ȶ��ԣ�R>W
B. X��Y�����γ�ԭ�Ӹ�����Ϊ1:1��1:2���������ӻ�����
C. ��X��Y��Z��W��R����Ԫ���γɵļ������а뾶��С����X2-
D. Y��Z��������������Ӧ��ˮ���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��ʵ�鱨����������ʵ�����ݣ��������ݺ������ǣ� ��
A.500 mL����ƿ����250 mL 0.1mol/L NaCl��Һ
B.����Ͳ��ȡ5.26 mL����
C.�ù㷺pH��ֽ�����Һ��pH��3.5
D.��25 mL�ζ�������15.80 mL��NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ⶨ����Ħ�������ʵ���У����������Ӱ��ⶨ������ǣ� ��
A.þ�����������Ĥδ��ȫ��ȥB.þ���к��в����ᷴӦ������
C.��Ӧ��û����ע��������D.���������þȫ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() Ϊ�����ӵ�������ֵ������˵����ȷ����
Ϊ�����ӵ�������ֵ������˵����ȷ����
A. 0.1 mol ��![]() ������
������![]() ������
������
B. pH=1��H3PO4��Һ�У�����![]() ��
��![]()
C. 2.24L����״��������O2����ȫȼ�գ��õ�![]() ��CO2����
��CO2����
D. �ܱ�������1 mol PCl3��1 mol Cl2��Ӧ�Ʊ� PCl5��g��������![]() ��P-Cl��
��P-Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Ӧ��ϵ�е������У�NaOH��Au2O3��Na2S4O6��Na2S2O3��Au2O��H2O��
(1)�뽫Au2O3֮��ķ�Ӧ����������ֱ��������¿ո��ڣ�________
![]()
![]()
(2)��Ӧ�У�����ԭ��Ԫ����______________����ԭ����___________��
(3)�뽫��Ӧ��Ļ�ѧʽ��ƽ���ϵ������������Ӧ��λ���У����������ת�Ƶķ������Ŀ��________
![]()
(4)��֯��ҵ�г���������Ư����Na2S2O3����ΪƯ�ײ�ƥ��ġ����ȼ�����Na2S2O3��Cl2��Ӧ�IJ�����H2SO4��NaCl��HCl����ԭ���������������ʵ���֮��Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���A�����ںϳɾ���������;���л���D��E������E�������࣬�ϳ�·�����£�

�ش��������⣺
��1��C�й����ŵ�����Ϊ_________________________________________��
��2��A����B�Ļ�ѧ����ʽΪ_____________________________________________��
��3��A����E�Ļ�ѧ����ʽΪ______________________________________________��
��4��A�ж���ͬ���칹�壬���к���̼��˫����ͬ���칹���У��˴Ź����������շ���Ŀ���ٵĽṹ��ʽ��_______________________________________��
��5������Ȳ�ͼ�ȩΪ��ʼԭ�ϣ�ѡ�ñ�Ҫ�����Լ��ϳ�1��3-����ϩ��![]() ����д���ϳ�·�ߣ��ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ��������_____
����д���ϳ�·�ߣ��ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ��������_____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����������仯��������ͼһ�µ���(����)

A. C + CO2![]() 2CO
2CO
B. CaCO3![]() CaO + CO2��
CaO + CO2��
C. 2Al + Fe2O3![]() 2Fe + Al2O3
2Fe + Al2O3
D. Ba(OH)2��8H2O + 2NH4Cl==BaCl2 + 2NH3��+ 10H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����͵��Ҵ���ؽṹ��ͼ��ʾ�����õ����������ܼ�����200������ʱ���磬��Ч�ʱȼ״���ظ߳�32�����Ҹ���ȫ����֪����ܷ�ӦʽΪC2H5OH+3O2�T2CO2+3H2O������˵������ȷ���ǣ�������
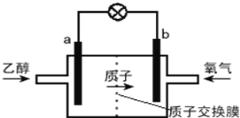
A. a��Ϊ��صĸ������õ缫����������Ӧ
B. ��ع���ʱ������a�������ص��߾����ݵ�b��
C. ��������ĵ缫��ӦʽΪ O2+2H2O+4e���T4OH��
D. ��ع���ʱ��1mol�Ҵ�������ת��12mol����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com