
在一定条件下,在一容积可变的密闭容器中,将SO2和O2混合发生反应:
2SO2(g)+O2(g)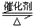 2SO3(g)
ΔH=-92.3KJ/mol,反应过程中,SO2、O2、SO3的物质的量(mol)的变化如下表(0~4min时,容器气体压强为0.1MPa):
2SO3(g)
ΔH=-92.3KJ/mol,反应过程中,SO2、O2、SO3的物质的量(mol)的变化如下表(0~4min时,容器气体压强为0.1MPa):
|
时间min |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
n(SO2) |
2.00 |
1.92 |
1.84 |
1.76 |
1.76 |
1.64 |
1.52 |
1.40 |
1.40 |
1.40 |
|
n(O2) |
1.00 |
0.96 |
0.92 |
0.88 |
0.88 |
0.82 |
0.76 |
0.70 |
0.70 |
0.70 |
|
n(SO3) |
0 |
0.08 |
0.16 |
0.24 |
0.24 |
0.36 |
0.48 |
0.60 |
0.60 |
0.60 |
回答下列问题:
(1)___________________________时段,反应处于平衡状态。
(2)第5min时,从同时提高速率和转化率两个方面分析,改变的外界条件是_____________;平衡向____________方向移动。(填“正”、“逆”或“不”)
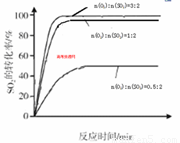
(3)其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图a。,Fe2O3和NiO作催化剂均能使S02的转化率达到最高,不考虑价格因素,选择Fe2O3的 主要优点是_____________。


(4)科研小组在3800C Fe2O3作催化剂时,研究了不同投料比n(O2):n(SO2)对S02转化率的影响,结果如图b。请在答题卡坐标图中画出n(O2):n(SO2)=1:2时,SO2转化率的预期变化曲线。
(1)3~4min(2分) 7~9min(2分)(2)增大压强(2分);正(2分)
(3)Cr2O3 (2分) Fe2O3作催化剂时,在相对较低温度可获得较高SO2的转化率。(2分)
(4)(3分)(标注1分,转折点1分,平台1分)
【解析】
试题分析:(1)由表格中的数据分析知,3~4min和7~9min时SO2、O2、SO3的物质的量保持不变,为化学平衡状态;(2)从表中数据分析,第5min时,SO2和O2的物质的量减小,SO3的物质的量增大,说明平衡向正向移动,该反应为放热反应,改变的条件可能为增大压强或降低温度,而降温反应速率变慢,从同时提高速率和转化率两个方面分析,改变的外界条件只能是增大压强;(3)由图像可知,当其他条件相同时,2600C以Cr2O3作催化剂,SO2的转化率最大,反应速率最快;对比分别以Fe2O3和NiO作催化剂的图像知,以Fe2O3作催化剂时,能在较低的温度下使SO2达到较高的转化率,因此选择Fe2O3;(4)分析图像b知,当SO2的物质的量相同时,O2的物质的量越大,达平衡的时间越短,反应速率越快,SO2的平衡转化率越大,以此可画出n(O2):n(SO2)=1:2时SO2转化率的预期变化曲线。
考点:考查化学平衡及平衡图像。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:阅读理解
 ),有关反应如下:
),有关反应如下:| c2(NO2) |
| C2(NO)c(O2) |
| c2(NO2) |
| C2(NO)c(O2) |


查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
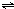 ClO(g)+3H2(g)△H>0.
ClO(g)+3H2(g)△H>0.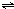 CH3OH(g)△H=-90.1kJ?mol-1,恒容条件下达平衡,下列措施中能使n(CH3OH)/n(CO)增大的有
CH3OH(g)△H=-90.1kJ?mol-1,恒容条件下达平衡,下列措施中能使n(CH3OH)/n(CO)增大的有
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
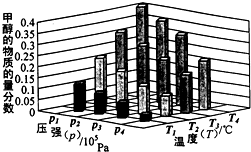 能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.
能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇可通过将煤的气化过程中生成的CO和H2在一定条件下发生如下反应制得:CO(g) + 2H2(g)=CH3OH(g)
请根据下图回答下列问题:
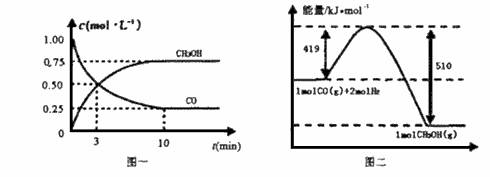
(1)从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)= 。
(2)写出该反应的热化学方程式 。
n(CH3OH)
(3)恒容条件下,下列措施中能使 n(CO) 增大的有 。
A.升高温度 B.充入He气 C.再充入1 mol CO和2 mol H2 D.使用催化剂
(4)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表:
| 容器 | 反应物投入的量 | 反应物的转化率 | CH3OH的浓度 | 能量变化(Q1、Q2、Q3均大于0) |
| 甲 | 1 mol CO和2 mol H2 | a1 | c1 | 放出Q1kJ热量 |
| 乙 | 1 mol CH3OH | a2 | c2 | 放出Q2kJ热量 |
| 丙 | 2mol CO和4 mol H2 | a3 | c3 | 放出Q3kJ热量 |
则下列关系正确的是:
A. c1=c2 B.2Q1=Q3 …… C.2a1=a3 D. a1+ a3=1
E.该反应若生成1 mol CH3OH,则放出(Q1+ Q2)kJ热量
(5)若在一体积可变的密闭容器中充入1 mol CO、2 mol H2和1 mol CH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则该反应向 (填“正”、“逆”)反应方向移动,理由是
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com