
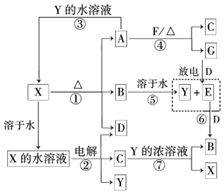
 A~G及X、Y均是中学化学常见物质,其中B、D、E、F、G在常温下为气体且B为红棕色,C的硫酸盐溶液通常为蓝色,它们之间有如下转化关系(其中反应③④⑦的产物中的水已略去).
A~G及X、Y均是中学化学常见物质,其中B、D、E、F、G在常温下为气体且B为红棕色,C的硫酸盐溶液通常为蓝色,它们之间有如下转化关系(其中反应③④⑦的产物中的水已略去).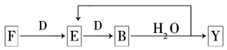
分析 B为红棕色气体,则B为NO2,二氧化氮溶于水得到硝酸和NO,E是气体,则E是NO、Y是HNO3,氮气和氧气放电生成NO,E能被D氧化生成B,则D是O2、G是N2,C是红色金属单质,为Cu,Cu和硝酸反应生成硝酸铜、NO,加热X能分解,则X是Cu(NO3)2,加热硝酸铜,硝酸铜分解生成CuO、二氧化氮和水,则A是CuO,
F是气体,CuO和F反应生成氮气、Cu,根据元素守恒知,F为NH3,结合题目分析解答.
解答 解:B为红棕色气体,则B为NO2,二氧化氮溶于水得到硝酸和NO,E是气体,则E是NO、Y是HNO3,氮气和氧气放电生成NO,E能被D氧化生成B,则D是O2、G是N2,C是红色金属单质,为Cu,Cu和硝酸反应生成硝酸铜、NO,加热X能分解,则X是Cu(NO3)2,加热硝酸铜,硝酸铜分解生成CuO、二氧化氮和水,则A是CuO,F是气体,CuO和F反应生成氮气、Cu,根据元素守恒知,F为NH3,
(1)G分子为氮气,氮原子间形成三键结构,结构式为:N≡N,故答案为:N≡N;
(2)⑦为Cu和浓硝酸反应生成硝酸铜、NO2和水的反应,该反应的离子方程式Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O,
故答案为:Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O;
(3)电解硝酸铜溶液时,阳极上氢氧根离子放电生成氧气,电极反应式为4OH--4e-=O2↑+2H2O,
故答案为:4OH--4e-=O2↑+2H2O;
(4)④为CuO和氨气在加热条件下反应生成氮气、Cu和水,所以该反应的化学方程式为3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$N2+3Cu+3H2O,
故答案为:3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$N2+3Cu+3H2O;
(5)F为氨气,Y为硝酸,氨气被氧气氧化生成NO,NO被氧气氧化生成二氧化氮,二氧化氮和水反应生成硝酸和NO,如果氨气经过一系列反应后完全转化为硝酸时,发生反应可以写为NH3+2O2=HNO3+H2O,根据方程式知消耗氨气和氧气的物质的量之比为1:2,
故答案为:1:2.
点评 本题以Cu、氮及其化合物为载体考查了无机物推断,以物质元素、状态、反应条件突破口采用正逆结合的方法进行推断,能正确书写离子方程式、电极反应式、化学方程式,注意(5)转移电子守恒的利用,题目难度中等.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | ⑤②④①③ | B. | ④②⑤①③ | C. | ②⑤④①③ | D. | ⑤④②①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16gO3所含的氧原子数目为NA | |
| B. | 标准状况下,22.4L H2O所含分子数目为NA | |
| C. | 24gMg变成Mg2+时失去的电子数目为NA | |
| D. | 1 L 1mol/L的FeCl3溶液中含有Cl-的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨常被用作制冷剂 | |
| B. | 可利用2Fe3++Cu═Cu2++2Fe2+腐蚀印刷电路板 | |
| C. | 为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质 | |
| D. | 已知3Cl2+8NH3═N2+6NH4Cl,工业上可用浓氨水检查氯气管道是否漏气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,用0.1000mol•L-1的盐酸滴定0.1000mol•L-1Na2CO3溶液25.00mL.用 pH传感器测得混合溶液的pH变化曲线如图,下列说法正确的是( )
常温下,用0.1000mol•L-1的盐酸滴定0.1000mol•L-1Na2CO3溶液25.00mL.用 pH传感器测得混合溶液的pH变化曲线如图,下列说法正确的是( )| A. | c→d发生的主要离子反应:HCO3-+H+=H2O+CO2 | |
| B. | 在b点 时,c(CO32-)>c(HCO3)->c(OH-) | |
| C. | 在d点 时,c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) | |
| D. | 在e点 时c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com