
���� ������ĵ���ƽ�ⳣ���жϸ��������ǿ��������������Ӷ�Ӧ�������Խǿ���ε�ˮ��̶�Խ����pH��ͬʱŨ��Խ�ݴ˽��н��
��� �⣺25��ʱ����֪Ka ��CH3COOH��=1.7��10-5mo1•L-1��Ka ��HCN��=4.93��10-10mo1•L-1��Ka1��H2CO3��=4.2��10-7mo1•L-1��Ka2��H2CO3��=5.6��10-11mo1•L-1��
�����Դ�СΪ��CH3COOH��H2CO3��HCN��HCO3-����
�����ζ���ǿ�������Σ�����������Ӷ�Ӧ�������Խǿ���ε�ˮ��̶�Խ����
��pH��ͬʱ�ٵ�Ũ����۵�Ũ����С���������Ӳ�ˮ�⣬��c��Na+����С��ϵΪ���ڣ��ۣ��٣�
�ʴ�Ϊ���ڣ��ۣ��٣�
���� ���⿼��������Ũ�ȴ�С�Ƚϣ���Ŀ�Ѷ��еȣ���ȷ�ε�ˮ�⼰��Ӱ��Ϊ���ؼ���ע��������Һ����ǿ�������ƽ�ⳣ���Ĺ�ϵ������������ѧ���ķ������������Ӧ��������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ͭ��ϡ���ᷴӦ��CuO+2H+=Cu2++H2O | |
| B�� | ϡ H2SO4�����۷�Ӧ��2Fe+6H+=2Fe3++3H2�� | |
| C�� | ����������Һ��ϡH2SO4 ��Ӧ��Ba2++SO42-=BaSO4�� | |
| D�� | �����ʯ��ˮ��ϡ���ᷴӦ��Ca��OH��2+2H+=Ca2++2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʵ���Ũ�ȵ�FeBr2��CuCl2�Ļ��Һ�ö��Ե缫������������Cu2++2Br-�TCu��+Br2 | |
| B�� | H218O��Ͷ��Na2O2��2H218O+2Na2O2�T4Na++4OH-+18O2�� | |
| C�� | ��������Һ����μ���Ba��OH��2��Һ��SO42-ǡ�ó�����ȫ�� 2Al3++3SO42-+3Ba2++6OH-�T2Al��OH��3��+3BaSO4�� | |
| D�� | Fe��NO3��3��������Һ��ͨ���������⣺2Fe3++H2S�T2Fe2++S��+2H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢܢݢߢ� | B�� | �ܢݢޢߢ� | C�� | �ڢܢޢߢ� | D�� | ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��C��s���ʯ��=C��sʯī����H=-1.19kJ/mol��֪ʯī�Ƚ��ʯ�ȶ� | |
| B�� | ���������������������ֱ���ȫȼ�գ�ǰ�߷ų��������� | |
| C�� | �Ȼ�ѧ����ʽ�еĻ�ѧ���������Ա�ʾ��ӳ���ʺ�������������� | |
| D�� | 2g H2��ȫȼ������Һ̬ˮ�ǽ��ų�285.8kJ���ȣ���˷�Ӧ���Ȼ�ѧ����ʽΪ2H2O��l��=2H2��g��+O2��l����H=-285.8KJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
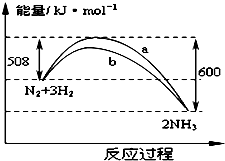 ��ͼ��425��ʱN2��H2��Ӧ�����������仯������ͼ������������ȷ���ǣ�������
��ͼ��425��ʱN2��H2��Ӧ�����������仯������ͼ������������ȷ���ǣ�������| A�� | �÷�Ӧ���Ȼ�ѧ����ʽΪ��N2+3H2?2NH3��H=-92kJ•mol-1 | |
| B�� | һ��������N2+3H2�T2NH3�ﵽƽ��ʱ��3v����H2��=2v����NH3�� | |
| C�� | ����������÷�Ӧ�ķ�Ӧ�ȷ����ı� | |
| D�� | �¶ȡ��������һ����ͨ��1molN2��3molH2��Ӧ��ų�������ΪQ1kJ����ͨ��2 molN2��6 molH2��Ӧ��ų�������ΪQ2kJ������184��Q2��2Q1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com