
下列有关金属腐蚀的叙述正确的是 ( )
A.金属越纯越不易被腐蚀
B.干燥环境下金属不被腐蚀
C.铜一定比铁难腐蚀
D.金属腐蚀有化学腐蚀和电化学腐蚀
科目:高中化学 来源: 题型:
下列实验操作不能达到预期目的的是 ( )
| 实验目的 | 操作 | |
| A | 欲比较水和乙醇中羟基氢的活泼性 | 用金属钠分别与水和乙醇反应 |
| B | 欲证明CH2=CHCHO中含有碳碳双键 | 滴加酸性KMnO4溶液,看紫红色是否褪去 |
| C | 欲确定磷、砷两元素非金属性的强弱 | 测定同温同浓度的Na3PO4和Na3AsO4水溶液的pH |
| D | 欲除去苯中混有的苯酚 | 向混合液中加入NaOH溶液,充分反应后,分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
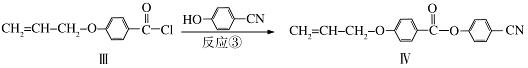
液晶高分子材料应用广泛,新型液晶基元﹣﹣化合物IV的合成线路如下:
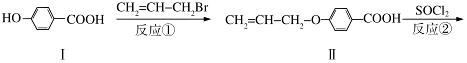
(1)化合物Ⅰ的分子式为 ,1mol化合物Ⅰ最多可与 mol NaOH反应。
(2)CH2=CH﹣CH2Br与NaOH水溶液反应的化学方程式为 (注明条件)。
(3)化合物I的同分异构体中,苯环上一溴代物只有2种且能发生银镜反应的化合物有多种,写出其中一种同分异构体的结构简式 (任写一种)。
(4)反应③的反应类型是 .在一定条件下,化合物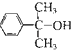 也可与III发生类似反应③的反应生成有机物V,V的结构简式是 。
也可与III发生类似反应③的反应生成有机物V,V的结构简式是 。
(5)下列关于化合物Ⅳ的说法正确的是 (填字母)。
A.属于烯烃 B.能与FeCl3溶液反应显紫色
C.一定条件下能发生加聚反应 D.能使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
工业废水中常含有一定量的Cr2O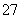 ,会对人类及生态系统产生很大损害,电解法是一种行之有效的除去铬的方法之一。该法用Fe作电极电解含Cr2O
,会对人类及生态系统产生很大损害,电解法是一种行之有效的除去铬的方法之一。该法用Fe作电极电解含Cr2O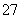 的酸性废水,最终将铬转化为Cr(OH)3沉淀,达到净化目的。下列有关说法不正确的是( )
的酸性废水,最终将铬转化为Cr(OH)3沉淀,达到净化目的。下列有关说法不正确的是( )
A.电解时选用Fe作阳极,石墨棒作阴极
B.阴极附近的沉淀只有Cr(OH)3
C.阳极附近溶液中,发生反应的离子方程式是Cr2O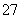 +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O
D.消耗1 mol Cr2O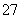 ,将有336 g Fe消耗,因此要定期更换铁电极
,将有336 g Fe消耗,因此要定期更换铁电极
查看答案和解析>>
科目:高中化学 来源: 题型:
镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型,NiMH中的M表示储氢金属或合金,该电池在充电过程中的总反应方程式是Ni(OH)2+M===NiOOH+MH。
已知:6NiOOH+NH3+H2O+OH-===6Ni(OH)2+NO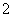
下列说法正确的是( )
A.NiMH电池放电过程中,正极的电极反应式为NiOOH+H2O+e-===Ni(OH)2+OH-
B.充电过程中OH-从阳极向阴极迁移
C.充电过程中阴极的电极反应式:H2O+M+e-===MH+OH-,H2O中的H被M还原
D.NiMH电池中可以用KOH溶液、氨水等作为电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生。某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1 mol/L FeCl2溶液,研究废液再生机理。记录如下(a、b、c代表电压值):
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(1)用KSCN溶液检验出Fe3+的现象是________。
(2)Ⅰ中,Fe3+产生的原因还可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应的离子方程式:________________________________________________。
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电。原因是Fe2+具有________性。
(4) Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:
Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
①NaCl溶液的浓度是________mol/L。
②Ⅳ中检验Cl2的实验方法:_____________________________________________________。
③与Ⅱ对比,得出的结论(写出两点):_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)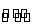 2NH3(g) ΔH=-92.4 kJ·mol-1。
2NH3(g) ΔH=-92.4 kJ·mol-1。
实验测得起始、平衡时的有关数据如下表:
| 容器 编号 | 起始时各物质物质的量/mol | 平衡时反应中 的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量akJ |
| ② | 2 | 3 | 0 | 放出热量bkJ |
| ③ | 2 | 6 | 0 | 放出热量ckJ |
下列叙述正确的是( )
A.放出热量关系:a<b<92.4
B.三个容器内反应的平衡常数:③>①>②
C.达平衡时氨气的体积分数:①>③
D.N2的转化率:②>①>③
查看答案和解析>>
科目:高中化学 来源: 题型:
在1-18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
| C | D | ||||||||
| A | B | E | F |
(1)画出D的原子结构示意图 ;
(2)写出C的最高价氧化物的电子式 ,该化合物所含化学键为 ;
(3)E和F分别形成的气态氢化物中最稳定的是 (填写氢化物的化学式);
(4)A最高价氧化物的水化物的化学式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com