
能源的开发利用与人类社会的可持续发展息息相关。
Ⅰ.已知:Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)
ΔH1=a kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH2=b kJ·mol-1
O2(g)=CO2(g) ΔH2=b kJ·mol-1
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH3=c kJ·mol-1
则C的燃烧热ΔH=________ kJ·mol-1。
Ⅱ.(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是________(填序号)。
A.C(s)+CO2(g)=2CO(g)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C.2H2O(l)=2H2(g)+O2(g)
D.2CO(g)+O2(g)=2CO2(g)
若以熔融的K2CO3与CO2为反应的环境,依据所选反应设计成一个原电池,请写出该原电池的负极反应:____________________________________________________________。
(2)某实验小组模拟工业合成氨反应N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1,开始他们将N2和H2混合气体20 mol(体积比1∶1)充入5 L合成塔中,反应前压强为p0,反应过程中压强用p表示,反应过程中
2NH3(g) ΔH=-92.4 kJ·mol-1,开始他们将N2和H2混合气体20 mol(体积比1∶1)充入5 L合成塔中,反应前压强为p0,反应过程中压强用p表示,反应过程中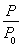 与时间t的关系如图所示。
与时间t的关系如图所示。

请回答下列问题:
①反应达平衡的标志是(填字母代号)________。
A.压强保持不变
B.气体密度保持不变
C.NH3的生成速率是N2的生成速率的2倍
②0~2 min内,以c(N2)变化表示的平均反应速率为________。
③欲提高N2的转化率,可采取的措施有________。
A.向体系中按体积比1∶1再充入N2和H2
B.分离出NH3
C.升高温度
D.充入氦气使压强增大
E.加入一定量的N2
(3)25 ℃时,BaCO3和BaSO4的溶度积常数分别是8×10-9和1×10-10,某含有BaCO3沉淀的悬浊液中,c(CO32-)=0.2 mol·L-1,如果加入等体积的Na2SO4溶液,若要产生BaSO4沉淀,加入Na2SO4溶液的物质的量浓度最小是________ mol·L-1。
Ⅰ. 
Ⅱ.(1)D CO-2e-+CO32-=2CO2
(2)①AC ②0.1 mol·L-1·min-1 ③AB (3)0.01
【解析】Ⅰ.三个热化学方程式依次编号为①、②、③,根据盖斯定律,(①×2+②×6+③)÷6得,C(s)+O2(g)=CO2(g) ΔH= (2a+6b+c)kJ·mol-1,则C的燃烧热为
(2a+6b+c)kJ·mol-1,则C的燃烧热为 kJ·mol-1。Ⅱ.(1)自发的氧化还原反应可以设计成原电池,选D;负极失电子发生氧化反应,负极反应为CO-2e-+CO32-=2CO2。(2)①此反应是反应前后气体分子数不相等的反应,压强不变说明达到平衡;因为气体总的质量不变,容器体积不变,所以密度始终不变,不能运用密度不变作为反应达到平衡的标志;NH3的生成速率是N2的生成速率的2倍,说明反应达到平衡。②设反应的N2为x mol,则反应的H2为3x mol,生成的NH3为2x mol,由压强关系得
kJ·mol-1。Ⅱ.(1)自发的氧化还原反应可以设计成原电池,选D;负极失电子发生氧化反应,负极反应为CO-2e-+CO32-=2CO2。(2)①此反应是反应前后气体分子数不相等的反应,压强不变说明达到平衡;因为气体总的质量不变,容器体积不变,所以密度始终不变,不能运用密度不变作为反应达到平衡的标志;NH3的生成速率是N2的生成速率的2倍,说明反应达到平衡。②设反应的N2为x mol,则反应的H2为3x mol,生成的NH3为2x mol,由压强关系得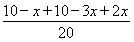 =0.9,解得x=1,则用氮气表示的平均反应速率为
=0.9,解得x=1,则用氮气表示的平均反应速率为 =0.1 mol·L-1·min-1。③此反应的正反应为放热反应,所以升高温度平衡逆向移动,氮气的转化率降低,C错误;充入氦气使压强增大,但各物质的浓度不变,平衡不移动,氮气的转化率不变,D错误;加入一定量的氮气,氮气的转化率降低,E错误。(3)根据题给数据,由Ksp(BaCO3)=
=0.1 mol·L-1·min-1。③此反应的正反应为放热反应,所以升高温度平衡逆向移动,氮气的转化率降低,C错误;充入氦气使压强增大,但各物质的浓度不变,平衡不移动,氮气的转化率不变,D错误;加入一定量的氮气,氮气的转化率降低,E错误。(3)根据题给数据,由Ksp(BaCO3)=
c(Ba2+)·c(CO32-)得c(Ba2+)=4×10-8 mol·L-1,混合后溶液中,c(Ba2+)=2×10-8 mol·L-1,要想产生BaSO4沉淀,至少需要Qc=c(Ba2+)·c(SO42-)=Ksp(BaSO4),计算得c(SO42-)=5×10-3 mol·L-1,则加入Na2SO4溶液的物质的量浓度最小是0.01 mol·L-1。


科目:高中化学 来源:2014学年高一化学人教版必修2 1.1.2元素的性质与原子结构练习卷(解析版) 题型:填空题
甲元素的原子序数是19,乙元素原子核外有两个电子层,最外电子层上有6个电子;丙是元素周期表第ⅠA族中金属性最弱的碱金属元素。由此推断:
(1)甲元素在周期表中位于第________周期;乙元素在周期表中位于第________族;丙元素的名称为________。
(2)甲的单质与水反应的离子方程式为____________________________;
乙单质与丙单质反应的化学方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮提分训练 专题1物质组成性质分类及化学用语练习卷(解析版) 题型:填空题
化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
(1)从物质的分类角度看,不恰当的一种物质是________(填物质名称)。
(2)“三酸”与“两碱”之间的反应,若用化学方程式表示有六个(酸过量时) ,若用离子方程式表示却只有两个,请写出这两个离子方程式:(酸过量时)_____________________________、______________________。
(3)“三酸”常用于溶解金属和金属氧化物。下列块状金属在常温时能全部溶于足量浓硝酸的是________。
A.Au B.Cu
C.Al D.Fe
(4)烧碱、纯碱溶液均可吸收CO2,当含0.1 mol NaOH的溶液吸收一定量CO2后,将溶液低温小心蒸干得到固体的组成可能有四种情况,分别是(填化学式):
①________,②Na2CO3,③________,④NaHCO3。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 高考模拟演练2练习卷(解析版) 题型:选择题
V、W、X、Y均是元素周期表中短周期元素,在周期表中的相对位置关系如表所示:
| Y | V |
|
|
X |
|
|
| W |
Z为第四周期常见元素,该元素是人体血液中血红蛋白最重要的组成金属元素。V的最简单氢化物为甲,W的最简单氢化物为乙,甲、乙混合时有白烟生成。下列说法正确的是( )。
A.原子半径:X>Y>V>W
B.X、W的质子数之和与最外层电子数之和的比值为2∶1
C.甲、乙混合时所生成的白烟为离子化合物,但其中含有共价键
D.少量Z的单质与过量W的单质可化合生成ZW2
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 高考模拟演练2练习卷(解析版) 题型:选择题
下列各组离子中,在给定条件下能大量共存的是( )。
A.在pH=1的溶液中,NH4+,K+,ClO-,Cl-
B.有SO42-存在的溶液中:Na+,Mg2+,Ba2+,I-
C.有NO3-存在的强酸性溶液中:NH4+,Ba2+,Fe2+,Br-
D.在c(H+)=1.0×10-13 mol·L-1的溶液中:Na+,S2-,AlO2-,SO32-
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 高考模拟演练1练习卷(解析版) 题型:选择题
下列有关溶液中微粒浓度关系的叙述正确的是( )。
A.向0.1 mol·L-1NH4Cl溶液中通入一定量氨气后:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.溶有等物质的量NaClO、NaHCO3的溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-)
C.向CH3COONa溶液中滴加稀盐酸至中性,所得溶液中:c(Cl-)>c(Na+)>c(CH3COOH)
D.等物质的量浓度CH3COOH溶液和CH3COONa溶液等体积混合,所得溶液中:c(CH3COOH)+2c(OH-)=2c(H+)+c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 高考模拟演练1练习卷(解析版) 题型:选择题
下列离子方程式书写不正确的是( )。
A.NaOH溶液与SO2反应,当n(NaOH)∶n(SO2)=4∶3时,4OH-+3SO2=SO32-+2HSO3-+H2O
B.CuCl2溶液与Na2S溶液2∶1反应:Cu2++S2-=CuS↓
C.Cl2与FeBr2溶液反应,当n(Cl2)∶n(FeBr2)=1∶1时:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
D.1 mol·L-1的NaAlO2溶液和2.5 mol·L-1的盐酸等体积互相均匀混合:2AlO2-+5H+=Al(OH)3↓+Al3++H2O
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 第9讲非金属元素及其化合物练习卷(解析版) 题型:选择题
物质间纷繁复杂的转化关系是化学的魅力所在,下列选项中物质的转化在一定条件下不能实现的是( )。
选项转化关系
A
B
C
D
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 第5讲化学反应与能量练习卷(解析版) 题型:填空题
(1)①根据下列图示,写出反应的热化学方程式___________________________。

②根据如图所示情况,判断下列说法中正确的是________。

A.其热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=41 kJ·mol-1
B.该反应为吸热反应
C.该反应为放热反应
D.当H2O为液态时,其反应热值小于41 kJ·mol-1
(2)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是________________________________________。
(3)如图是某温度下,N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为_________________________________。

a、b两条曲线产生区别的原因很可能是_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com