
【题目】在温度不变的条件下,在恒容的容器中进行下列反应:N2O4(g)=2NO2(g),若N2O4的浓度由0.1mol/L降到0.07mol/L需要15s,那么N2O4的浓度由0.07mol/L降到0.05mol/L所需的反应时间( )
A. 等于5s B. 等于10s C. 小于10s D. 大于10s
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】人类对原子结构的探究经历了多个历史阶段.下列各阶段的先后顺序正确的是( )
①徳谟克利特提出的古典原子论 ②道尔顿提出的近代原子论
③卢瑟福提出原子结构的行星模型 ④汤姆逊提出原子结构的“葡萄干面包模型”
A.①②③④B.①②④③C.①③④②D.④③①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】支撑海港码头基础的钢管柱,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极.下列有关表述不正确的是( )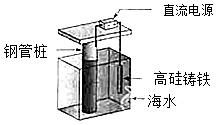
A.通入保护电流使钢管桩表面腐蚀电流接近于零
B.通电后外电路电子被强制从高硅铸铁流向钢管桩
C.高硅铸铁的作用是作为损耗阳极材料和传递电流
D.通入的保护电流应该根据环境条件变化进行调整
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液的体积比为3:2:1时,则三种溶液中Cl-的物质的量之比为( )
A. 3:4:3 B. 1:2:3 C. 3:2:1 D. 1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表达下列反应的离子方程式为( )
A.用醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
B.硫化亚铁与浓硫酸混合加热:2H++FeS=H2S↑+ Fe2+
C.向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3 ![]() =Al2(CO3)3↓
=Al2(CO3)3↓
D.用氢氧化钠溶液吸收工业废气中的NO2:2NO2+2OH= ![]() +
+ ![]() + H2O
+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)Li4Ti3O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为Fe TiO3 , 还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:
回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如下图所示.由图可知,当铁的净出率为70%时,所采用的实验条件为 . 
(2)“酸浸”后,钛主要以TiOCl42﹣形式存在,写出相应反应的离子方程式 .
(3)TiO2xH2O沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
温度/℃ | 30 | 35 | 40 | 45 | 50 |
TiO2xH2O转化率/% | 92 | 95 | 97 | 93 | 88 |
分析40℃时TiO2xH2O转化率最高的原因 .
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为 .
(5)若“滤液②”中c(Mg2+)=0.02molL﹣1 , 加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1.0×10﹣5 , 此时是否有Mg3(PO4)2沉淀生成?(列式计算).FePO4、Mg3(PO4)2的分别为1.3×10﹣22、1.0×10﹣24
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对放热反应:A+B═C+D,以下说法一定正确的是(EA、EB、EC、ED分别表示物质A,B,C,D所具有的能量)( )
A.EA>EB
B.EA>EB+EC
C.EA+EB>EC+ED
D.EA+EB<EC+ED
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个固定容积的密闭容器中,可逆反应m A(g)+n B(g)![]() p C(g)+q D(g),当 m、 n、 p、q 为任意整数时,下列说法一定能说明反应已达到平衡的是( )
p C(g)+q D(g),当 m、 n、 p、q 为任意整数时,下列说法一定能说明反应已达到平衡的是( )
①体系的压强不再改变 ②体系的密度不再改变 ③各组分的浓度不再改变 ④各组分的质量分数不再改变 ⑤反应速率 v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q ⑥单位时间内 m mol A 发生断键反应,同时 p mol C 也发生断键反应
A. ③④⑤⑥ B. ③④⑥ C. ①③④ D. ②③⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com