
| A. | 都是银白色的柔软金属(除铯外) | |
| B. | 密度都比较小 | |
| C. | 碱金属单质都与水剧烈反应 | |
| D. | 单质的熔、沸点随原子序数的增加而升高 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 将16.0g CuSO4溶于100mL水中 | |
| B. | 将25.0g CuSO4•5H2O溶于少量水中,再用水稀释至100mL | |
| C. | 将20mL5.0mol/L CuSO4溶液用水稀释至100mL | |
| D. | 在20mL5.0mol/L CuSO4溶液中加入80mL水 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
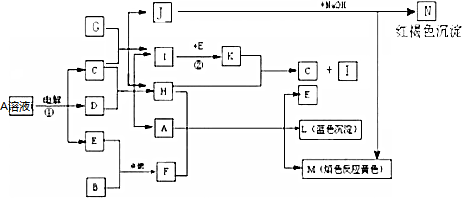
 ,写出其与CO2反应的化学方程式并用双线桥标出电子转移的方向和数目
,写出其与CO2反应的化学方程式并用双线桥标出电子转移的方向和数目 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图的实验装置可用于实验室中制取乙炔.请回答下列问题:
如图的实验装置可用于实验室中制取乙炔.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
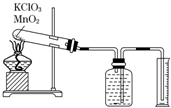 某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2.
某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在气体发生装置上直接点燃一氧化碳气体时,必须要先检验一氧化碳气体的纯度,最简单的方法是用排空气的方法先收集一试管气体,点燃气体,听爆鸣声 | |
| B. | 进行蒸馏操作时,冷凝管中的冷凝水应从上口进,下口出 | |
| C. | 萃取操作时,振荡过程中需要放气,通过旋转分液漏斗的上口的玻璃活塞进行 | |
| D. | 将饱和FeCl3溶液滴入沸水中,继续加热煮沸,并用玻璃棒不断搅拌直至体系呈红褐色即得Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期期中化学试卷(解析版) 题型:选择题
稀硫酸和系硝酸的混合液,其中H2SO4和HNO3的物质的量浓度分别是4mol/L和2mol/L,取10ml此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体的体积为(设反应中HNO3倍还原成NO)
A.0.672L B.0.448L C.0.896L D.0.224L
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.甲酸甲酯的结构简式:CH2O
B.Na+的结构示意图: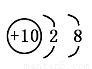
C.质子数为53、中子数为78的碘原子:13153I
D.CO2的电子式: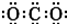
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com