
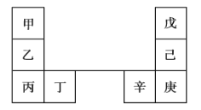
【题目】甲~辛元素在周期表中的相对位置如图所示。甲和戊的原子序数相差3,戊的一种单质是自然界中硬度最大的物质,丁和辛属同周期元素。下列判断正确的是( )
A.金属性:甲![]() 乙
乙![]() 丁
丁
B.原子半径:庚![]() 己
己![]() 戊
戊
C.丙和庚的原子核外电子数相差12
D.乙的单质在空气中燃烧生成只含离子键的化合物
【答案】B
【解析】
戊的一种单质是自然界硬度最大的物质,则戊为C元素;己、庚与C与戊同主族,二者分别为Si、Ge元素;甲和戊的原子序数相差3,甲的原子序数为6-3=3,为Li元素,乙、丙与Li同主族,二者分别为Na、K元素;然后结合各元素的相对位置可知:丁为Ca元素,辛为Ga元素,据此解答。
根据分析可知,甲为Li,乙为Na,丙为K,丁为Ca,戊为C元素,己为Si,庚为Ge,辛为Ga元素。
A.根据元素周期律可知,同主族元素从上到下金属性逐渐增强,则金属性:甲<乙,结合金属活动性顺序表可知,金属性Ca>Na,则金属性:甲<乙<丁,故A错误;
B.电子层数越多,原子半径越大,则原子半径:庚>己>戊,故B正确;
C.丙的原子序数是19,庚的原子序数是32,则原子的核外电子数的差值也即原子序数的差值,丙与庚的原子核外电子数相差13,故C错误;
D.Na在空气中燃烧生成过氧化钠,过氧化钠既含离子键又含共价键,D故错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】(15 分)化合物H 是合成药物盐酸沙格雷酯的重要中间体,其合成路线如下:
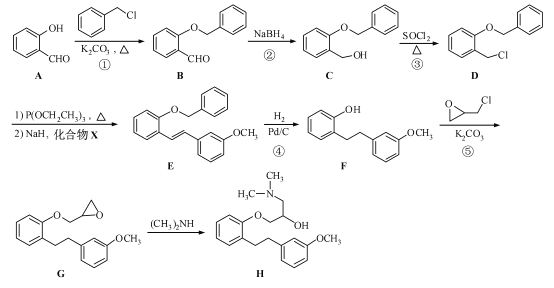
(1)化合物A 中的含氧官能团为 和 (填官能团名称)。
(2)反应①→⑤中,属于取代反应的是 (填序号)。
(3)写出同时满足下列条件的B 的一种同分异构体的结构简式: 。
I. 分子中含有两个苯环;II. 分子中有7 种不同化学环境的氢;III. 不能与FeCl3溶液发生显色反应,但水解产物之一能发生此反应。
(4)实现D→E 的转化中,加入的化合物X 能发生银镜反应,X 的结构简式为 。
(5)已知:![]() 。化合物
。化合物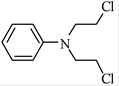 是合成抗癌药物美法伦的中间体,请写出以
是合成抗癌药物美法伦的中间体,请写出以![]() 和
和![]() 为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下。
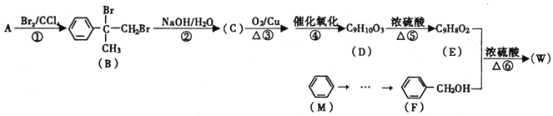
请回答下列问题:
(1)F的化学名称是________,⑤的反应类型是________。
(2)E中含有的官能团是________(写名称),D聚合生成高分子化合物的结构简式为________。
(3)将反应③得到的产物与O2在催化剂、加热的条件下反应可得D,写出反应④的化学方程式________。
(4)④、⑤两步能否颠倒?________(填“能”或“否”)理由是________。
(5)与A具有含有相同官能团的芳香化合物的同分异构体还有________种(不含立体异构),其中核磁共振氢谱为六组峰,且峰面积之比为1:1:2:2:2:2的结构简式为________。
(6)参照有机物W的上述合成路线,以M和CH3Cl为原料制备F的合成路线(无机试剂任选)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素原子半径与原子序数的关系图。字母代表元素,分析正确的是
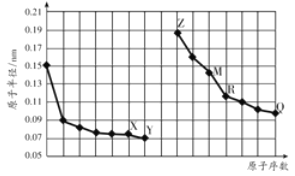
A. R在周期表的第15列
B. Y、Q两种元素的气态氢化物及其最高价氧化物的水化物均为强酸
C. 简单离子的半径:X>Z>M
D. Z的单质能从M与Q元素构成的盐溶液中置换出单质M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,把SiO2细粉放入蒸馏水中,搅拌至平衡,生成H4SiO4溶液(SiO2+2H2OH4SiO4),该反应平衡常数K随温度的变化如图示,搅拌1小时,测得H4SiO4的质量分数为0.01%(溶液密度为1.0g/mL),下列分析正确的是( )
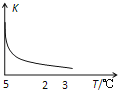
A.该反应平衡常数的表达式为K=c(H4SiO4)
B.该生成H4SiO4的反应为吸热反应
C.用H4SiO4表示的反应速率为1.04×10﹣2mol/(Lh)
D.若K值变大,在平衡移动时逆反应速率先减小后增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与下列事实对应的化学用语错误是( )
A.纯碱溶液能清洗油污:CO32﹣+H2OHCO3﹣+OH﹣
B.配制FeSO4溶液时加入适量的铁粉:Fe3++Fe→2Fe2+
C.含1molNaOH和1molNa2CO3的混合溶液中滴入含1.5molHCl的稀盐酸:2OH﹣+CO32﹣+3H+→HCO3﹣+2H2O
D.NH4Al(SO4)2溶液中滴入Ba(OH)2溶液至SO42﹣恰好沉淀完全:2Ba2++4OH﹣+Al3++2SO42﹣→2BaSO4↓+AlO2﹣+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 五种元素的原子结构,回答下列问题:
五种元素的原子结构,回答下列问题:
(1)只有![]() 层与
层与![]() 层的原子有______;
层的原子有______;
(2)含有![]() 层的原子有______;
层的原子有______;
(3)最外层电子数相同的原子有______;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有四种元素的基态原子的电子排布式:
①![]() ; ②
; ②![]() ;
;
③![]() ; ④
; ④![]() 。
。
则下列有关比较中正确的是
A. 电负性:④>③>②>① B. 原子半径:④>③>②>①
C. 第一电离能:④>③>②>① D. 最高正化合价:④>③=②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成是一个需要经历多步反应的过程,我们常用的塑料包装绳(主要成分为聚氯乙烯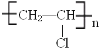 就是通过多步反应生产出来的。现在有1,2-二溴乙烷,氢氧化钠醇溶液、二氧化锰、锌粒、稀硫酸等主要原料,请您设计反应的步骤得到聚氯乙烯,将每一步反应的化学方程式写出__________________________________
就是通过多步反应生产出来的。现在有1,2-二溴乙烷,氢氧化钠醇溶液、二氧化锰、锌粒、稀硫酸等主要原料,请您设计反应的步骤得到聚氯乙烯,将每一步反应的化学方程式写出__________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com