
科目:高中化学 来源: 题型:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
| c(N2)c2(CO2) |
| c2(CO)c2(NO) |
| c(N2)c2(CO2) |
| c2(CO)c2(NO) |
查看答案和解析>>
科目:高中化学 来源: 题型:
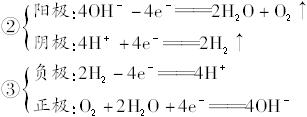
燃料电池实验装置
②按下开关S1,接通电源,电解溶液约半分钟,碳棒上发生明显的气泡。
③断开开关S1,按下开关S2,接通二极管,观察实验现象。
实现现象:____________________________________________________________。
有关的电极反应:
②__________________________________________________________________。
③__________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
[s1] (1)实验室里需用480 mL 0.1 mol/L的CuSO4溶液,①以下配制方法正确的是 。
A.称取7.68 g CuSO4加入500 mL水
B.称取12.0 g胆矾加入500 mL水
C.称取8.0 g CuSO4加入500 mL水
D.称取12.5 g胆矾配成500 mL溶液
②假如其他操作均准确无误,分析下列情况对配制浓度的影响
A.定容时俯视观察刻度线: ;
B.移液时,对用于溶解CuSO4(或胆矾)的烧杯没有洗涤: ;
C.定容后,将容量瓶振荡摇匀,静置时发现液面低于刻度线,又补加水至刻度线: 。
(2)用98%(密度为1.84 g/cm3)的浓硫酸稀释成3 mol/L的稀硫酸100 mL,回答下列问题:
①需要浓硫酸 mL;
②配制操作可分解成如下几步,正确的操作顺序是 。
A.向容量瓶中注入少量水,检查是否漏水
B.用少量蒸馏水洗涤烧杯及玻璃棒,将溶液注入容量瓶,并重复操作两次
C.将已冷却的稀硫酸注入已检查不漏水的容量瓶中
D.根据计算,用量筒量取一定体积的浓硫酸
E.将浓硫酸沿烧杯壁慢慢注入盛有蒸馏水的小烧杯中,并不断用玻璃棒搅拌
F.盖上容量瓶塞子,振荡,摇匀
G.用胶头滴管滴加蒸馏水,使溶液凹液面恰好与刻度线相切
H.缓缓地将蒸馏水注入容量瓶内,直到容量瓶中的液面接近容量瓶刻度1 cm~2 cm处
[s1]11.
查看答案和解析>>
科目:高中化学 来源:2010年高三备考“好题速递”系列(21) 题型:填空题
[s1] (1)若某药品质量约为32.0 g,用托盘天平准确称其质量,若用↓表示在右盘放上砝码,用↑表示将砝码取下,在下列表格的空格内,用↓和↑表示相应砝码的放上或取下。
|
50 g |
20 g |
20 g |
10 g |
5 g |
|
|
|
|
|
|
 |
(3)在配制一定物质的量浓度的溶液时,用“偏高、偏低、无影响”表示下列操作对所配溶液浓度的影响。
①用量筒量取液态溶质,读数时,俯视量筒,所配制溶液的浓度 。
②将量取液态溶质的量筒用水洗涤,洗涤液倒入容量瓶,所配制溶液的浓度 。
③定容摇匀后,有少量溶液外流,对所配制溶液的浓度 。
[s1]12.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com