
LiPF6������ӵ���й㷺Ӧ�õĵ���ʡ�ij������LiF��PCl5Ϊԭ�ϣ����·�Ӧ�Ʊ�LiPF6�����������£�
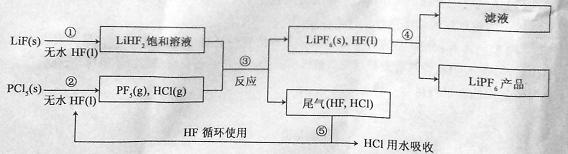
��֪��HCl�ķе��ǣ�85.0 �棬HF�ķе���19.5 �档
��1���ڢٲ���Ӧ����ˮHF�������� �� ����Ӧ�豸�����ò������ʵ�ԭ���� (�û�ѧ����ʽ��ʾ)����ˮHF�и�ʴ�ԺͶ��ԣ�������ȫ�ֲ���ʾ�������С�Ľ�HFմ��Ƥ���ϣ���������2%�� ��Һ��ϴ��
��2��������������ˮ�����½��У��ڢ۲���Ӧ��PCl5����ˮ�⣬�����Ϊ�����ᣬд��PCl5ˮ��Ļ�ѧ����ʽ�� ��
��3���ڢܲ�������õķ����� ���ڢݲ�����β����HF��HCl���õķ����� ��
��4��LiPF6��Ʒ��ͨ����������LiF��ȡ��Ʒwg�����Li�����ʵ���Ϊnmol�������Ʒ��LiPF6�����ʵ���Ϊ mol(�ú���w��n�Ĵ���ʽ��ʾ)��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ױ������ϵ�һ��Hԭ�ӱ�ʽ��Ϊ43��������ȡ�����õ���һԪȡ���������
A. 7�� B. 6�� C. 4�� D. 3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧʽΪC8H10O�Ļ�����A�����������ʣ�
 |
��A��Na���������������ݡ� ��A��RCOOH ����ζ�IJ���
 �����������ﲻ�ܷ���������Ӧ
�����������ﲻ�ܷ���������Ӧ
����ˮ��Ӧ�IJ�����ۺϷ�Ӧ���Ƶ�һ������Ʒ(����Ŀǰ��ɡ���ɫ��Ⱦ������Ҫ
��ȾԴ֮һ)
��1������������Ϣ���Ըû�����Ľṹ���������ж��� ��
A.������ֱ�������ǻ� B.��������ĩ���м� C.�϶��д��ǻ� D.�϶��Ƿ�����
��2��������A�Ľṹ��ʽΪ ��
��3��A�ͽ����Ʒ�Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£�������Һ������Ũ�ȴ�С��ϵ��ȷ����
A��Na2S��Һ��c(Na+)>c(HS-)>c(OH-)>c(H2S)
B��Na2C2O4��Һ�У�c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4)
C��Na2CO3��Һ��c(Na+)+c(H+)=2c(CO32-)+c(OH-)
D��CH3COONa��CaCl2�����Һ��c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ҷ����Ԫ�صļ���ɾ��������ĸ��������,��������ѡ�õ�ʵ����Ʒ���ܶ��õ�����( )


A������Ҷ���ջһ���ѡ�â١��ں͢�
B����Ũ�����ܽ��Ҷ�Ҳ�������ˮϡ�ͣ�ѡ�âܡ��͢�
C�����˵õ�����Һ��ѡ�âܡ��ݺ͢�
D��������Һ�е�Fe3����ѡ�âۡ���͢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������Ҫ������Դ��������Ϊ�������õĹؼ��������ǵ�ǰ��ע���ȵ�֮һ��
�������������Դ����ȼ�ղ���Ϊ ��
��NaBH4��һ����Ҫ�Ĵ������壬����ˮ��Ӧ����NaBO3���ҷ�Ӧǰ��B�Ļ��ϼ۲��䣬�÷�Ӧ�Ļ�ѧ����ʽΪ����Ӧ����1molNaBH4ʱת�Ƶĵ�����ĿΪ��
�Ǵ���ɽ����л�������û�����ͱ�֮��Ŀ��淴Ӧ��ʵ������ͼ��⡣

 (g)
(g)


 (g)��3H2(g)
(g)��3H2(g)
��ij�¶��£�����������м��뻷���飬����ʼŨ��Ϊamol��L��1��ƽ��ʱ����Ũ��Ϊbmol��L��1���÷�Ӧ��ƽ�ⳣ��K��
��һ�������£���11ͼ��ʾװ�ÿ�ʵ���л���ĵ绯ѧ���⣨���������л����


�ٵ����е���ת�Ʒ���Ϊ ������A��D��ʾ��
������Ŀ�����ĵ缫��ӦʽΪ ��
�۸ô���װ�õĵ���Ч�ʦǣ� �����ǣ�����Ŀ��������ĵĵ�����/ת�Ƶĵ���������100%������������С�����1λ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������ˮ�����г�����ɱ��������HClO��ɱ��������ClO��ǿ��25��ʱ����-��ˮ��ϵ�д�������ƽ���ϵ��
Cl2(g)  Cl2(aq) K1=10��1.2
Cl2(aq) K1=10��1.2
Cl2(aq)+ H2O  HClO + H+ +Cl�� K2=10��3.4
HClO + H+ +Cl�� K2=10��3.4
HClO  H+ + ClO�� Ka=?
H+ + ClO�� Ka=?
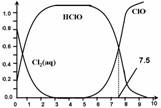 ����Cl2(aq)��HClO��ClO���ֱ�����������ռ����(��)��pH�仯�Ĺ�ϵ��ͼ��ʾ�����б�����ȷ����
����Cl2(aq)��HClO��ClO���ֱ�����������ռ����(��)��pH�仯�Ĺ�ϵ��ͼ��ʾ�����б�����ȷ����
A��Cl2(g)+ H2O  2H+ + ClO�� + Cl�� K=10��10.9
2H+ + ClO�� + Cl�� K=10��10.9
B�����ȴ���ˮ��ϵ�У�c(HClO) + c(ClO��) =c(H+)��c(OH��)
C�����ȴ�������ˮʱ��pH=7.5ʱɱ��Ч����pH=6.5ʱ��
D���ȴ�������ˮʱ�����ļ���ɱ��Ч�����ڶ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���б仯�����������仯���� (����)
A��ʣ������ B�����г�����
C��ţ�̱��� D����Ʒ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com