
| A. | 按系统命名法,有机物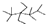 的命名为2,2,4,4,5-五甲基-3,3-二乙基己烷 的命名为2,2,4,4,5-五甲基-3,3-二乙基己烷 | |
| B. | 人造纤维,合成纤维都是有机高分子化合物 | |
| C. | 某有机物含有C、H、O、N四种元素,其球棍模型为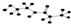 ,该有机物的结构简式为 ,该有机物的结构简式为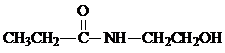 | |
| D. | 红斑素、红曲素是常用于糖果、雪糕等食品的着色剂的主要成分,结构分别如下图所示: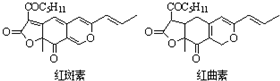 则红斑素和红曲素互为同分异构体 |
分析 A.选取最长碳链为主链,从离取代基近的一端编号,保证取代基位次和最小,确定取代基位置写出名称;
B.相对分子质量在10000以上的有机化合物为高分子化合物;
C.根据原子成键方式知,该有机物结构简式为HO-CH2-CH2-NH-CO-CH2-CH3;
D.根据红斑素和红曲素的结构及分子组成进行判断;
解答 解:A.按系统命名法,有机物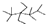 的 命名为2,2,4,4,5-五甲基-3,3-二乙基己烷,故A正确;
的 命名为2,2,4,4,5-五甲基-3,3-二乙基己烷,故A正确;
B.人造纤维,合成纤维相对分子质量在10000以上,都是有机高分子化合物,故B正确;
C.根据原子成键方式知,能形成4个共价键的原子是C原子、能形成1个共价键的原子是H原子、能形成3个共价键的是N原子、能形成2个共价键的是O原子,所以该有机物结构简式为HO-CH2-CH2-NH-CO-CH2-CH3,故C正确;
D.红斑素含有5个碳碳双键,而红曲素含有3个碳碳双键,其他结构相同,因此含有的氢原子数不同,所以它们的分子式不同,一定不是同分异构体,故D错误.
故选D.
点评 本题考查较为综合,涉及高分子化合物概念、烷烃命名、同分异构体、球棍模型等知识,为高频考点,侧重于学生的分析能力和基础知识的综合理解和运用的考查,难度中等,注意相关知识的积累.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
| A. | 只有难溶电解质才存在沉淀溶解平衡过程 | |
| B. | 沉淀溶解平衡过程是可逆的 | |
| C. | 在平衡状态时v溶解=v结晶=0 | |
| D. | 达到沉淀溶解平衡的溶液一定是饱和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯分子中的所有原子可能共平面 | |
| B. | CH2═CH-C6H5分子中的所有原子可能共平面 | |
| C. | 乙烷分子中的所有原子可能共平面 | |
| D. | 二氯甲烷分子为正四面体结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
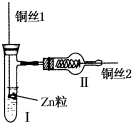 如图为氢气还原氧化铜的微型快速实验装置.实验前先将铜丝1处理成下端弯曲的小圆环,并用铁锤击成带小孔的小匙,将铜丝2一端弯曲成螺旋状.试回答下列问题:
如图为氢气还原氧化铜的微型快速实验装置.实验前先将铜丝1处理成下端弯曲的小圆环,并用铁锤击成带小孔的小匙,将铜丝2一端弯曲成螺旋状.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
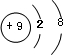 ,该元素与金属性最强的元素形成的化合物的电子式为
,该元素与金属性最强的元素形成的化合物的电子式为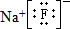 ;该化合物中存在的化学键为离子键 (选填“离子键”或“共价键”).
;该化合物中存在的化学键为离子键 (选填“离子键”或“共价键”).查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 X、Y、Z、W、R五种元素位于元素周期表前四周期,它们的原子序数依次增大
X、Y、Z、W、R五种元素位于元素周期表前四周期,它们的原子序数依次增大| 元素 | 相关信息 |
| X | 原子核外的价电子排布式为nsnnp2n |
| Y | 元素周期表中电负性最强的元素 |
| Z | Z与W位于同周期,且最外层有两个未成对电子 |
| w | 单质为淡黄色固体,能在火山口发现 |
| R | 原子的基态未成对电子致是同周期最多的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 A、B、C、D、E五种元素均位于前四周期,原子序数逐渐增大,只有两种是金属元素.A、B、D三种元素在周期表中相对位置如图,其中A的价层电子排布为ns2np3,C的基态原子的第I电离能远小于第II电离能.E是第四期第IB族元素,回答下列问题:
A、B、C、D、E五种元素均位于前四周期,原子序数逐渐增大,只有两种是金属元素.A、B、D三种元素在周期表中相对位置如图,其中A的价层电子排布为ns2np3,C的基态原子的第I电离能远小于第II电离能.E是第四期第IB族元素,回答下列问题:| A | B | |
| D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 定醛 | B. | 丙醛 | C. | 乙醛 | D. | 甲醛 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com