
| A. | B一定为气体 | |
| B. | A一定为气体 | |
| C. | 若正反应方向△H<0,则T1>T2 | |
| D. | 压强增大时,混合气体的平均相对分子质量减小 |
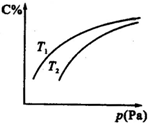
分析 采取定一议二方式解答,由图可知,温度一定时,压强越大,C的含量越大,故增大压强平衡向正反应移动,故B一定为气体;压强一定时,温度越高,平衡向吸热方向移动,根据C的含量变化结合选项判断反应热与温度高低.
解答 解:A、温度一定时,压强越大,C的含量越大,故增大压强平衡向正反应移动,正反应是气体体积减小的反应,即B一定是气体,故A正确;
B、由C中的分析可知,B一定是气体,A可能是气体,可能为非气体,故B错误.
C、若正反应方向△H<0,升高温度,平衡向逆反应移动,C的含量降低,由图可知,温度T2到达平衡时C的含量较低,故温度T2>T1,故C错误;
D、温度一定时,压强越大,C的含量越大,平衡向正反应方向移动,A、B至少有一种气体,而A的化学计量数小于C,故B一定为气体,若均为气体,混合气体总质量不变,总的物质的量减少,平均相对分子质量增大,若A为非气态,平衡正向移动,混合气体的总质量增大,总的物质的量减少,故平均相对分子质量增大,故D错误;
故选A.
点评 本题考查外界条件对化学反应速率、化学平衡移动影响、学生识图能力,难度不大,做题时注意分析图象曲线的变化特点,采取定一议二解答.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
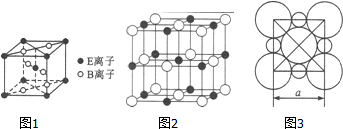 A、B、C、D、E五种常见元素的核电荷数依次增大.A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物,E的基态3d轨道上有2个电子.请回答下列问题:
A、B、C、D、E五种常见元素的核电荷数依次增大.A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物,E的基态3d轨道上有2个电子.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4个 | B. | 5个 | C. | 6个 | D. | 7个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
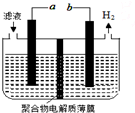 某研究小组利用电化学方法处理石油炼制过程中产生的含H2S的废气.基本工艺是将H2S通入FeCl3溶液中,过滤后将滤液加入如图所示电解槽中电解,电解后的滤液可以循环利用.下列有关说法正确的是( )
某研究小组利用电化学方法处理石油炼制过程中产生的含H2S的废气.基本工艺是将H2S通入FeCl3溶液中,过滤后将滤液加入如图所示电解槽中电解,电解后的滤液可以循环利用.下列有关说法正确的是( )| A. | 过滤得到的沉淀可能是FeS | |
| B. | 与a极相连的电极反应式为Fe2+-e-═Fe3+ | |
| C. | 可以用Fe与外接电源的a极相连 | |
| D. | 若有0.1mol电子发生转移,则一定能得到1.12LH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Mg、Cu、Ag | B. | K、Al、Zn、Fe | C. | Na、Zn、Fe、Cu | D. | Cu、Ag、Fe、Na |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x+y<z | B. | 平衡向正反应方向移动 | ||
| C. | B的转化率降低 | D. | C的产率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用饱和NaCl溶液除去Cl2中的HCl | |
| B. | 乙酸乙酯在碱性条件下水解更充分 | |
| C. | 工业合成氨反应:N2(g)+3H2(g)?2NH3 (g)△H=-92.4kJ/mol,采用较高的温度下进行 | |
| D. | 接触法制硫酸工业中通入过量空气与SO2反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com