
 “æĶŌŚ¹¤ŅµÉĻÖ÷ŅŖÓĆĄ“ÖĘŌģµ¼Ļß”¢µēĘ÷ŌŖ¼žµČ£¬ĶÄÜŠĪ³É+1ŗĶ+2µÄ»ÆŗĻĪļ£®»Ų“šĻĀĮŠĪŹĢā£ŗ
“æĶŌŚ¹¤ŅµÉĻÖ÷ŅŖÓĆĄ“ÖĘŌģµ¼Ļß”¢µēĘ÷ŌŖ¼žµČ£¬ĶÄÜŠĪ³É+1ŗĶ+2µÄ»ÆŗĻĪļ£®»Ų“šĻĀĮŠĪŹĢā£ŗ·ÖĪö £Ø1£©CuµÄŌ×ÓŠņŹżĪŖ29£¬¼Ūµē×ÓÅŲ¼ĪŖ3d104s1£»C”¢O”¢NŌŖĖŲ¶¼ŹĒµŚ¶žÖÜĘŚ·Ē½šŹōŌŖĖŲ£¬Ķ¬Ņ»ÖÜĘŚŌŖĖŲ×Ō×ó¶ųÓŅµŚŅ»µēĄėÄܳŹŌö“óĒ÷ŹĘ£¬µ«NŌŖĖŲŌ×Ó2pÄܼ¶ŹĒ°ėĀśĪȶØדĢ¬£¬ÄÜĮæ½ĻµĶ£¬µŚŅ»µēĄėÄÜøßÓŚĶ¬ÖÜĘŚĻąĮŚŌŖĖŲ£¬¾Ż“Ė“šĢā£»
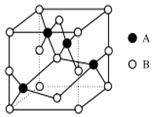
£Ø2£©Óɾ§°ūŹ¾ŅāĶ¼æÉÖŖ£¬1øö¾§°ūÖŠÓŠ4øöA£¬BĪŖ8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$=4øö£»
£Ø3£©NH3ÖŠNŌ×ÓĢį¹©¹Ā¶Ōµē×Ó£¬Cu2+Ģį¹©æÕ¹ģµĄ£¬ŠĪ³ÉÅäĪ»¼ü£»NH3·Ö×ÓÖŠ¹Ā¶Ōµē×ÓŹżĪŖ1£¬³É¼üŹżĪŖ3£¬ÓėNH3·Ö×Ó»„ĪŖµČµē×ÓĢåµÄŅ»ÖÖĪ¢Į£¾ßÓŠĻąĶ¬µÄ¼Ūµē×ÓŹżŗĶŌ×ÓŹż£®
½ā“š ½ā£ŗ£Ø1£©CuµÄŌ×ÓŠņŹżĪŖ29£¬¼Ūµē×ÓÅŲ¼ĪŖ3d104s1£¬Ōņ»łĢ¬Cu2+µÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ[Ar]3d9£¬C”¢O”¢NŌŖĖŲ¶¼ŹĒµŚ¶žÖÜĘŚ·Ē½šŹōŌŖĖŲ£¬Ķ¬Ņ»ÖÜĘŚŌŖĖŲ×Ō×ó¶ųÓŅµŚŅ»µēĄėÄܳŹŌö“óĒ÷ŹĘ£¬µ«NŌŖĖŲŌ×Ó2pÄܼ¶ŹĒ°ėĀśĪȶØדĢ¬£¬ÄÜĮæ½ĻµĶ£¬µŚŅ»µēĄėÄÜøßÓŚĶ¬ÖÜĘŚĻąĮŚŌŖĖŲ£¬¹ŹµŚŅ»µēĄėÄÜN£¾O£¾C£¬
¹Ź“š°øĪŖ£ŗ[Ar]3d9£»N£¾O£¾C£»
£Ø2£©Óɾ§°ūŹ¾ŅāĶ¼æÉÖŖ£¬1øö¾§°ūÖŠÓŠ4øöA£¬BĪŖ8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$=4øö£¬Ō×ÓøöŹżÖ®±ČĪŖ1£ŗ1£¬øĆŃõ»ÆĪļµÄ»ÆѧŹ½ĪŖCuO£¬¹Ź“š°øĪŖ£ŗCuO£»
£Ø3£©NH3ÖŠNŌ×ÓĢį¹©¹Ā¶Ōµē×Ó£¬Cu2+Ģį¹©æÕ¹ģµĄ£¬¶žÕߊĪ³ÉÅäĪ»¼ü£¬NH3·Ö×ÓÖŠ¹Ā¶Ōµē×ÓŹżĪŖ1£¬³É¼üŹżĪŖ3£¬ŌņNŌ×ÓµÄŌӻƷ½Ź½ĪŖsp3£¬ÓėNH3·Ö×Ó»„ĪŖµČµē×ÓĢåµÄŅ»ÖÖĪ¢Į£¾ßÓŠĻąĶ¬µÄ¼Ūµē×ÓŹż8ŗĶŌ×ÓŹż4£¬Ī¢Į£ĪŖPH3»ņH3O+µČ£¬¹Ź“š°øĪŖ£ŗsp3£»PH3»ņH3O+µČ£®
µćĘĄ ±¾Ģāæ¼²é½Ļ×ŪŗĻ£¬Éę¼°µē×ÓÅŲ¼”¢¾§°ū¼ĘĖć”¢ŌӻƷ½Ź½”¢µČµē×ÓĢåµČ£¬²ąÖŲŌ×Ó½į¹¹ÓėŠŌÖŹµÄ漲飬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČĖ¹¤·Ö×ÓÉø£Ø¶ąæ×¹čĀĮĖįŃĪ£©æÉŅŌÓĆ×÷Īüø½¼ĮŗĶ“߻ƼĮ | |
| B£® | ¹č½ŗæÉŅŌÓĆ×÷Ź³Ę·”¢Ņ©Ę·µÄøÉŌļ¼Į | |
| C£® | ĄūÓĆ·ēÄÜ”¢Ģ«ŃōÄܵČÄÜŌ““śĢę»ÆŹÆČ¼ĮĻ£¬ÓŠĄūÓŚ½ŚŌ¼ÄÜŌ“±£»¤»·¾³ | |
| D£® | ²ĻĖ攢ėęĀŚŗĶµÓĀŚ¼ČŹōÓŚ»ÆѧĻĖĪ¬ÓÖŹōÓŚøß·Ö×Ó»ÆŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Li | B£® | Na | C£® | Mg | D£® | K |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HCHO | B£® | CH3COOCH2CH3 | C£® | HOOCCOOH | D£® | HCOOH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ¢Ł | ¢Ś | ¢Ū | ¢Ü |
| 0.1mol/LNaOHČÜŅŗ | pH=11NaOHČÜŅŗ | 0.1mol/L CH3COOHČÜŅŗ | pH=3CH3COOHČÜŅŗ |
| A£® | ÓÉĖ®µēĄė³öH+µÄÅضČc£ØH+£©£ŗ¢Ł£¾¢Ū | |
| B£® | ½«¢Ü¼ÓÕōĮóĖ®Ļ”ŹĶÖĮŌĄ“µÄ100±¶Ź±£¬ĖłµĆČÜŅŗµÄPH£¾5 | |
| C£® | ¢ŁÓė¢Ū»ģŗĻ£¬ČōČÜŅŗpH=7£¬ŌņĢå»ż£ŗV£ØNaOH£©£¾V£ØCH3COOH£© | |
| D£® | µČĢå»żµČPHµÄ¢ÜČÜŅŗŗĶŃĪĖį·Ö±šÓė×ćĮæµÄZn·“Ó¦£¬¢ÜČÜŅŗÉś³ÉĶ¬Ģõ¼žĻĀĒāĘųĢå»ż¶ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ČõĖį | CH3COOH | H2CO3 | HNO2 |
| µēĄė³£Źż | K=1.8”Į10-5 | K=4.3”Į10-7 K=5.6”Į10-11 | K=5.0”Į10-4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
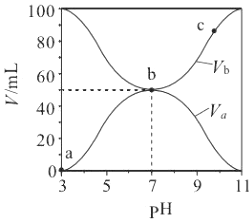
| A£® | Ka£ØHA£©µÄÖµÓė Kb£ØBOH£© µÄÖµ²»ĻąµČ | |
| B£® | b µćŹ±£¬Ė®µēĄė³öµÄ c£ØH+£©=10-7mol/L | |
| C£® | c µćŹ±£¬c£ØA-£©£¾c£ØB+£© | |
| D£® | a”śc ¹ż³ĢÖŠ$\frac{c£Ø{A}^{-}£©}{c£ØO{H}^{-}£©•c£ØHA£©}$²»±ä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
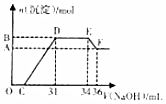 ĻõĖįŌ½Ļ”»¹Ō²śĪļÖŠµŖŌŖĖŲµÄ»ÆŗĻ¼ŪŌ½µĶ£®Ä³Ķ¬Ń§Č”ĢśĀĮŗĻ½šÓė×ćĮæŗÜĻ”µÄĻõĖį³ä·Ö·“ӦƻӊĘųĢå·Å³ö£®ŌŚ·“Ó¦ŗóµÄČÜŅŗÖŠÖš½„¼ÓČė4mol•L-1NaOHČÜŅŗ£¬Ėł¼ÓNaOHČÜŅŗµÄĢå»żÓė²śÉśµÄ³ĮµķµÄĪļÖŹµÄĮæµÄ¹ŲĻµČēĶ¼ĖłŹ¾£Ø²»æ¼ĀĒ³ĮµķµÄĪ¢ĮæČܽā£©£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ĻõĖįŌ½Ļ”»¹Ō²śĪļÖŠµŖŌŖĖŲµÄ»ÆŗĻ¼ŪŌ½µĶ£®Ä³Ķ¬Ń§Č”ĢśĀĮŗĻ½šÓė×ćĮæŗÜĻ”µÄĻõĖį³ä·Ö·“ӦƻӊĘųĢå·Å³ö£®ŌŚ·“Ó¦ŗóµÄČÜŅŗÖŠÖš½„¼ÓČė4mol•L-1NaOHČÜŅŗ£¬Ėł¼ÓNaOHČÜŅŗµÄĢå»żÓė²śÉśµÄ³ĮµķµÄĪļÖŹµÄĮæµÄ¹ŲĻµČēĶ¼ĖłŹ¾£Ø²»æ¼ĀĒ³ĮµķµÄĪ¢ĮæČܽā£©£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | DµćČÜŅŗÖŠ“ęŌŚ£ŗc£ØNH4+£©+c£ØNa+£©+c£ØH+£©ØTc£ØOH-£©+c£ØNO3-£© | |
| B£® | EF¶Ī·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗAl£ØOH£©3+OH-ØTAlO2-+2H2O | |
| C£® | DµćČÜŅŗÖŠn£ØNH4+£©=0.012mol | |
| D£® | ÓÉĖ®µēĄė²śÉśµÄc£ØH+£©£ŗOµć£¾Fµć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
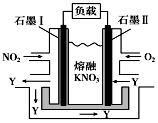 Ä³Č¼ĮĻµē³ŲµÄ¹¤×÷ŌĄķČēÓŅĶ¼ĖłŹ¾£¬øƵē³ŲŌŚŹ¹ÓĆ¹ż³ĢÖŠŹÆÄ«¢ńµē¼«ÉĻÉś³ÉŃõ»ÆĪļY£¬YæÉŃ»·Ź¹ÓĆ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
Ä³Č¼ĮĻµē³ŲµÄ¹¤×÷ŌĄķČēÓŅĶ¼ĖłŹ¾£¬øƵē³ŲŌŚŹ¹ÓĆ¹ż³ĢÖŠŹÆÄ«¢ńµē¼«ÉĻÉś³ÉŃõ»ÆĪļY£¬YæÉŃ»·Ź¹ÓĆ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | øƵē³Ų·ÅµēŹ±K+ĻņŹÆÄ«¢ńµē¼«ĒØŅĘ | |
| B£® | ŹÆÄ«¢ńø½½ü·¢ÉśµÄ·“Ó¦£ŗNO2-e-+NO3-ØTN2O5 | |
| C£® | O2ŌŚŹÆÄ«¢ņø½½ü·¢ÉśŃõ»Æ·“Ó¦£¬YĪŖNO | |
| D£® | ĻąĶ¬Ģõ¼žĻĀ£¬·Åµē¹ż³ĢÖŠĻūŗĵÄNO2ŗĶO2µÄĢå»ż±ČĪŖ2£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com