
| A�� | ������ˮ�������c��H+��•c��OH-��=10-20����Һ�У�Na+��Cl-��S2-��SO32- | |
| B�� | �μ���ɫ��̪����Ϊ��ɫ����Һ��Na+��CO32-��K+��ClO-��SO42- | |
| C�� | ���루NH4��2Fe��SO4��2•6H2O�������Һ�У�Na+��H+��Cl-��NO3- | |
| D�� | �����£�pH��7����Һ�У�I-��SO42-��Al3+��K+ |
���� A��������ˮ�������c��H+��•c��OH-��=10-20����ҺΪ���Ի�ǿ������Һ�������ӡ�������������������ӷ�Ӧ��
B���μ���ɫ��̪����Ϊ��ɫ����ҺΪ������Һ��̼������ӡ������������ֻ�ܴ����ڼ�����Һ��
C������������������������ܹ������������ӣ�
D��pHС��7����ҺΪ������Һ����������֮�䲻��Ӧ�������������ӷ�Ӧ��
��� �⣺A��������ˮ�������c��H+��•c��OH-��=10-20����Һ��ˮ�����������Ũ��Ϊc��H+��=c��OH-��=10-10mol/L����Һ�д��ڵ��������ӻ����������ӣ�S2-��SO32-�������ӷ�Ӧ����������Һ�в��ܴ������棬��A����
B������ҺΪ������Һ��CO32-��ClO-ֻ�ܴ����ڼ�����Һ������Һ�в��ܴ������棬��B����
C����NH4��2Fe��SO4��2•6H2O�ܹ�������������ӣ�H+��NO3-�ܹ������������ӣ�����Һ�в��ܴ������棬��C����
D��������pH��7����Һ�д��ڴ��������ӣ�I-��SO42-��Al3+��K+֮�䲻��Ӧ�������������ӷ�Ӧ������Һ���ܹ��������棬��D��ȷ��
��ѡD��
���� ���⿼�����ӹ���������жϣ�Ϊ�߿��ĸ�Ƶ�⣬��Ŀ�Ѷ��еȣ�ע����ȷ���Ӳ��ܴ��������һ��������磺�ܷ������ֽⷴӦ������֮�䣻�ܷ���������ԭ��Ӧ������֮��ȣ���Ӧ��ע����Ŀ���������������磺��Һ������ԣ��ݴ����ж���Һ���Ƿ��д����� H+��OH-����Һ�ľ��巴Ӧ�������硰������ԭ��Ӧ�������������۲������������ǡ����ܡ����棬���ǡ�һ��������ȣ�


 �ľ�ͼ���ʱ�ȷ�ϵ�д�
�ľ�ͼ���ʱ�ȷ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1��1 | B�� | 1��2��4 | C�� | 1��2��3 | D�� | 1��3��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
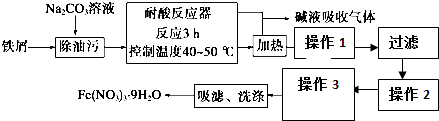
| ���� | Cu��OH��2 | Fe��OH��3 |
| Ksp | 2.2��10-20 | 2.6��10-39 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2O2�����������ӵĸ�����Ϊ1��1 | |
| B�� | Na2O2�ֱ���ˮ��CO2��Ӧ������ͬ����O2ʱ����Ҫˮ��CO2��������� | |
| C�� | Na2O2�ֱ���ˮ��CO2��Ӧ������ͬ����O2ʱ����Ҫˮ��CO2�����ʵ������ | |
| D�� | Na2O2��Ư��ԭ�������̿��Ư��ԭ����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���顢������������Һ������ʹ���Ը��������Һ��ɫ | |
| B�� | CH��CH��CH2=CHCH=CH2��Ϊͬϵ�� | |
| C�� | ���������ڼ��������µ�ˮ�ⷴӦ������Ӧ | |
| D�� | 2��2-����������2��4-���������һ�ȴ���������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
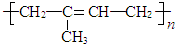 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 7.8 g Na2O2��������ʪ��CO2��Ӧ��ת�Ƶĵ�����Ϊ0.1 NA | |
| B�� | ��״����2.24 L HCHO�к�0.4 NA��ԭ�� | |
| C�� | 23.4g NaCl�����к�0.1 NA����ͼ��ʾ�ṹ��Ԫ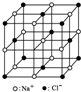 | |
| D�� | 4.0gSiC�����к��еĹ��ۼ���ĿΪ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
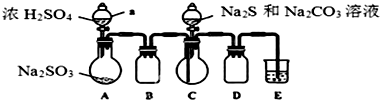
| ʵ�鲽�� | Ԥ���������� |
| ����1��ȡ����������Ʒ������������ˮ�� | ������ȫ�ܽ����ɫ������Һ |
| ����2������������� | |
| ����3�����ú�ȡ����Һ������BaCl2��Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com