
| A. | 氢氧化钡溶液与稀硫酸混合:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | 少量SO2通入到漂白粉溶液中:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO | |
| C. | 氯化铝溶液与过量的氨水反应:Al3++4NH3•H2O=AlO2-+4NH4++2H2O | |
| D. | 往明矾溶液中加入氢氧化钡溶液至SO42-完全沉淀:Al3++2SO42-+2 Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
分析 A.不符合离子的配比;
B.发生氧化还原反应生成硫酸钙;
C.反应生成氢氧化铝和氯化铵;
D.至SO42-完全沉淀,以1:2反应生成硫酸钡、偏铝酸钾和水.
解答 解:A.氢氧化钡溶液与稀硫酸混合的离子反应为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故A错误;
B.少量SO2通入到漂白粉溶液中的离子方程式为Ca2++2ClO-+SO2+H2O=CaSO4+H++Cl-+HClO,故B错误;
C.氯化铝溶液与过量的氨水反应的离子反应为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故C错误;
D.往明矾溶液中加入氢氧化钡溶液至SO42-完全沉淀的离子反应为Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应的考查,题目难度不大.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 原固体混合物中Cu与Cu2O的物质的量之比为1:1 | |
| B. | 原稀硝酸中HNO3的物质的量浓度为1.3mol•L-l | |
| C. | 产生的NO的体积为2.24L | |
| D. | Cu、Cu2O与硝酸反应后剩余HNO3为0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

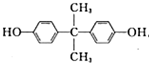 ,G是一种高分子,可用于制造隐形眼镜的材料.H为六元环酯.
,G是一种高分子,可用于制造隐形眼镜的材料.H为六元环酯. .
. .
. .
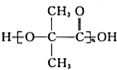
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Fe2+、SO42-、NO3- | B. | Mg2+、K+、Cl-、AlO2- | ||
| C. | Al3+、Na+、SO42-、HS- | D. | Ca2+、H+、NO3-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
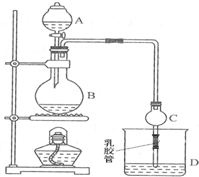 已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH.
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH.| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
 CH3COOCH2CH3+H218O.
CH3COOCH2CH3+H218O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com