

| A、滤液A中的阳离子为Fe2+、Fe3+、H+ |
| B、V=224 |
| C、样品中CuO的质量为2.0g |
| D、样品中Fe元素的质量为1.07g |
| 2.88g-1.6g-1.12g |
| 16g/mol |


 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案科目:高中化学 来源: 题型:
| A、该反应的平衡常数K=c ([CoCl4]2-)2/[c (Co2+)?c (Cl-)4] |
| B、升高温度,正反应速率增大,逆反应速率减小 |
| C、将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为蓝色 |
| D、增大Cl-浓度,平衡向正反应方向移动,Co2+、Cl-浓度都减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
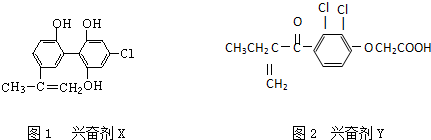
| A、1 mol兴奋剂X与足量浓溴水反应,最多消耗5 mol Br2 |
| B、1 mol兴奋剂Y与足量NaOH溶液反应,最多消耗3 mol NaOH |
| C、两种兴奋剂遇FeCl3溶液均显色,均属于苯酚的同系物 |
| D、兴奋剂X所有碳原子有可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去AgI胶体中混有的I-离子--过滤、洗涤、干燥 |
| B、除去苯中含有的少量苯酚--加入NaOH溶液、分液 |
| C、分离CuSO4?5H2O和BaSO4的混合物--溶解、过滤 |
| D、除去乙酸乙酯中混有的乙酸杂质--加入NaOH溶液、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(N2)=0.40mol?L-1?s-1 |
| B、v(H2)=0.80mol?L-1?s-1 |
| C、v(NH3)=0.60mol?L-1?s-1 |
| D、v(NH3)=1.20mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,28g N2和CO的混合气体体积为22.4L | ||
| B、任何物质的摩尔质量等于它的相对原子质量或相对分子质量 | ||
C、一个钠原子的质量约为
| ||
| D、CO2的摩尔质量为44g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com