
·ÖĪö ¢Ł°±Ęų·Ö½āĪŖģŲŌöµÄ·“Ó¦£¬øł¾Ż”÷G=”÷H-T”÷S£¼0£¬·“Ó¦æÉŅŌ×Ō·¢½ųŠŠ£»
¢ŚĄÕĻÄĢŲĮŠŌĄķĪŖ£ŗČē¹ūøıäÓ°ĻģĘ½ŗāµÄĢõ¼žÖ®Ņ»£¬Ę½ŗā½«Ļņ×ÅÄܹ»¼õČõÕāÖÖøıäµÄ·½ĻņŅĘ¶Æ£¬Ź¹ÓĆĄÕĻÄĢŲĮŠŌĄķŹ±£¬øĆ·“Ó¦±ŲŠėŹĒæÉÄę·“Ó¦£¬·ńŌņĄÕĻÄĢŲĮŠŌĄķ²»ŹŹÓĆ£»
¢Ūøł¾ŻŃ¹ĒæÖ®±ČµČÓŚĪļÖŹµÄĮæÖ®±Č¼ĘĖć³öĘ½ŗāŗ󣬻ģŗĻĘųĢåµÄĪļÖŹµÄĮ棬ĄūÓĆ²īĮæ·Ø¼ĘĖć²Ī¼Ó·“Ó¦µÄµŖĘųµÄĪļÖŹµÄĮæ£¬Ę½ŗā³£ŹżÖøÉś³ÉĪļÅØ¶ČµÄ»Æѧ¼ĘĮæŹż“ĪĆŻµÄ³Ė»ż³żŅŌø÷·“Ó¦ĪļÅØ¶ČµÄ»Æѧ¼ĘĮæŹż“ĪĆŻµÄ³Ė»żĖłµĆµÄ±ČÖµ£®
½ā“š ½ā£ŗ¢Ł”÷G=”÷H-T”÷S£¼0£¬·“Ó¦æÉŅŌ×Ō·¢½ųŠŠ£¬°±Ęų·Ö½āĪŖģŲŌöµÄ·“Ó¦£¬ĒŅ”÷HĪŖŌö“ó·“Ó¦£¬¹Ź·“Ó¦ŌŚøßĪĀĻĀæÉŅŌ×Ō·¢½ųŠŠ£¬
¹Ź“š°øĪŖ£ŗøßĪĀ£»
¢Śa”¢ÓĆĢś“„Ć½¼Óæģ»Æѧ·“Ó¦ĖŁĀŹ£¬ŹĒĄūÓĆĢś“„Ć½×ö“߻ƼĮ½µµĶ·“Ó¦µÄ»ī»ÆÄÜ£¬¼Óæģ·“Ó¦ĖŁĀŹ£¬²»øıä»ÆŃ§Ę½ŗā£¬²»ÄÜÓĆĄÕĻÄĢŲĮŠŌĄķ½āŹĶ£¬¹Ź²»·ūŗĻ£»
b”¢·“Ó¦ŹĒĘųĢåĢå»ż¼õŠ”µÄ·“Ó¦£¬¼ÓŃ¹Ę½ŗāÕżĻņ½ųŠŠ·ūŗĻ»ÆŃ§Ę½ŗāŅʶÆŌĄķ£¬æÉŅŌÓĆĄÕĻÄĢŲĮŠŌĄķ½āŹĶ£¬¹Ź·ūŗĻ£»
c”¢ŗĻ³É°±·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶Č²»ĄūÓĆĘ½ŗāĻņÕż·½ĻņŅĘ¶Æ£¬µ«ÉżĪĀČ“æÉĢįøß·“Ó¦ĖŁĀŹ£¬“߻ƼĮ»īŠŌ“ó£¬ÓėĄÕɳĢŲĮŠŌĄķ²»·ū£¬¹Ź²»·ūŗĻ£»
d”¢½«Éś³ÉµÄ°±Ņŗ»Æ²¢¼°Ź±“ÓĢåĻµÖŠ·ÖĄė³öĄ“£¬¼õÉŁÉś³ÉĪļÅØ¶Č£¬Ę½ŗāÕżĻņ½ųŠŠ£¬æÉŅŌÓĆĄÕĻÄĢŲĮŠŌĄķ½āŹĶ£¬¹Ź·ūŗĻ£»
¹ŹŃ”£ŗbd£»
¢Ū·“Ó¦“ļµ½Ę½ŗāŹ±£¬ČŻĘ÷ÄŚĘųĢåµÄŃ¹ĒæĪŖĘšŹ¼Ź±µÄ80%£¬ĖłŅŌĘ½ŗāŹ±»ģŗĻĘųĢåµÄĪļÖŹµÄĮæĪŖ£Ø1.5mol+3.5mol£©”Į80%=4mol£¬Éč²Ī¼Ó·“Ó¦µÄµŖĘųµÄĪļÖŹµÄĮæŹĒx£¬
¶ŌÓŚ·“Ó¦£ŗN2£Øg£©+3H2£Øg£©?2NH3£Øg£©
³õŹ¼ÅØ¶Č£ŗ1.5 3.5 0
±ä»ÆÅØ¶Č£ŗx 3x 2x
Ę½ŗāÅØ¶Č£ŗ1.5-x 3.5-3x 2x
ĖłŅŌ1.5-x+3.5-3x+2x=4£¬½āµĆx=0.5mol£¬·“Ó¦Ę½ŗā³£Źżk=$\frac{{1}^{2}}{1”Į{2}^{3}}$=0.125£Ømol/L£©-2£®
¹Ź“š°øĪŖ£ŗ0.125£Ømol/L£©-2£®
µćĘĄ ±¾Ģā漲鷓Ӧ×Ō·¢ŠŌÅŠ¶Ļ”¢»Æѧ·“Ó¦ĖŁĀŹ¼°»ÆŃ§Ę½ŗāÓ°ĻģŅņĖŲ£¬²ąÖŲæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦”¢¶ŌÖŖŹ¶µÄÓ¦ÓĆÄÜĮ¦£¬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĻ©ŗĶ±½¶¼æÉŅŌ“ÓĆŗ½¹ÓĶÖŠ»ńµĆ | |
| B£® | ŅŅĻ©ŗĶ±½¶¼ŹĒĘ½Ćę½į¹¹£¬ŅņĪŖ¶žÕß·Ö×ÓÖŠ¶¼ŗ¬ÓŠĢ¼Ģ¼Ė«¼ü | |
| C£® | ŅŅĻ©ŗĶ±½¶¼ÄÜŹ¹äåĖ®ĶŹÉ«£¬ĒŅĶŹÉ«µÄŌŅņĻąĶ¬ | |
| D£® | ŅŅĻ©ŗĶ±½¶¼ÄÜÓėH2·¢Éś¼Ó³É·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ūĻ©ĖįæÉŅŌ·¢ÉśČ”“ś·“Ó¦ | |
| B£® | ±ūĻ©ĖįæÉŅŌŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ« | |
| C£® | ±ūĻ©ĖįÓėHBr·¢Éś¼Ó³É·“Ó¦Ö»ÄܵƵ½ĪØŅ»²śĪļ | |
| D£® | ±ūĻ©ĖįÄĘČÜŅŗÖŠNa+ÅØ¶Č“óÓŚ±ūĻ©ĖįøłĄė×ÓÅØ¶Č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū¢Ü | B£® | ¢Ü¢Ż¢Ž | C£® | ¢Ś¢Ū¢Ž | D£® | ¢Ł¢Ū¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²śĪļBµÄדĢ¬Ö»ÄÜĪŖ¹ĢĢ¬»ņŅŗĢ¬ | |
| B£® | Ę½ŗāŹ±£¬µ„Ī»Ź±¼äÄŚn£ØA£©ĻūŗÄ©sn£ØC£©ĻūŗÄ=1©s1 | |
| C£® | ČōæŖŹ¼Ź±ĻņČŻĘ÷ÖŠ¼ÓČė1molBŗĶ1molC£¬“ļµ½Ę½ŗāŹ±·Å³öČČĮæµČÓŚQ kJ | |
| D£® | ±£³ÖĢå»ż²»±ä£¬ĻņĘ½ŗāĢåĻµÖŠ¼ÓČėA£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
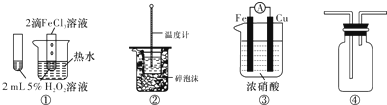
| A£® | Ķ¼¢ŁæÉŃéÖ¤FeCl3¶ŌH2O2·Ö½ā·“Ó¦ÓŠ“ß»Æ×÷ÓĆ | |
| B£® | Ķ¼¢ŚæÉÓĆÓŚÖŠŗĶČČµÄ²ā¶Ø | |
| C£® | Ķ¼¢ŪæÉÓĆÓŚĢ½¾æĢś×÷øŗ¼«µÄŌµē³ŲŌĄķ | |
| D£® | Ķ¼¢ÜæÉÓĆÓŚŹÕ¼ÆNH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ | B£® | x+y£¾z | ||
| C£® | CµÄĢå»ż·ÖŹżŌö“ó | D£® | BµÄ×Ŗ»ÆĀŹŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
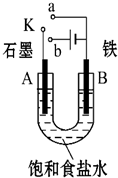 ijæĪĶā»ī¶ÆŠ”×éÓĆČēĶ¼×°ÖĆ½ųŠŠŹµŃ飬ŹŌ»Ų“šĻĀĮŠĪŹĢā£®
ijæĪĶā»ī¶ÆŠ”×éÓĆČēĶ¼×°ÖĆ½ųŠŠŹµŃ飬ŹŌ»Ų“šĻĀĮŠĪŹĢā£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
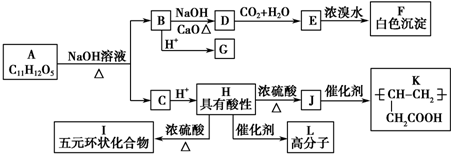
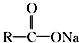 +NaOH$”ś_{”÷}^{CaO}$RØTH+Na2CO3
+NaOH$”ś_{”÷}^{CaO}$RØTH+Na2CO3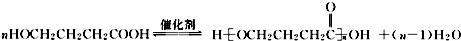 £®
£® £®
£®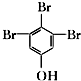 £ØŠ“½į¹¹¼ņŹ½£©£®
£ØŠ“½į¹¹¼ņŹ½£©£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com