
【题目】某小组的同学们利用如图装置,探究不同条件对铁与酸反应速率的影响. 
请回答下列问题.
(1)铁与稀硫酸反应的离子方程式是 .
(2)适当升高烧瓶内液体的温度,产生气泡的速率将(填“加快、”“减慢”或“不变”),由此得出的结论是 .
(3)将稀硫酸换为浓硫酸,可观察到 , 原因是 .
(4)向烧瓶中滴入几滴CuSO4溶液,产生气泡的速率明显加快.这是什么原因? 甲同学:CuSO4溶液中的Cu2+对铁与稀硫酸的反应起了催化作用.
乙同学:CuSO4与Fe反应生成了Cu,从而Fe、Cu、稀硫酸构成了原电池,使反应速率加快.
你同意的观点,欲证明此观点,可另取一套上图装置,向烧瓶中直接加入少量 , 观察现象.
【答案】
(1)Fe+2H+=Fe2++H2↑
(2)加快;升温可使铁与酸的反应速率加快
(3)铁的表面没有气泡;浓硫酸将铁钝化
(4)乙;铜粉
【解析】解:(1)铁和稀硫酸反应生成硫酸亚铁和氢气,反应的离子方程式为:Fe+2H+=Fe2++H2↑; 所以答案是:Fe+2H+=Fe2++H2↑;(2)升温加快化学反应速率,故产生气泡的速率将加快;由此得出的结论是升温可使铁与酸的反应速率加快,所以答案是:加快;升温可使铁与酸的反应速率加快;(3)浓度越大化学反应速率越快,但是铁与浓硫酸会发生钝化反应,故将稀硫酸换为浓硫酸,可观察到铁的表面没有气泡;原因是浓硫酸将铁钝化,所以答案是:铁的表面没有气泡; 浓硫酸将铁钝化;(4)构成原电池可加快化学反应速率,故同意乙的观点;欲证明此观点,可另取一套上图装置,向烧瓶中直接加入少量铜粉,目的是构成Fe﹣Cu原电池,所以答案是:乙; 铜粉.


科目:高中化学 来源: 题型:
【题目】合成氨反应为:N2(g)+3H2(g)![]() 2NH3(g)。图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。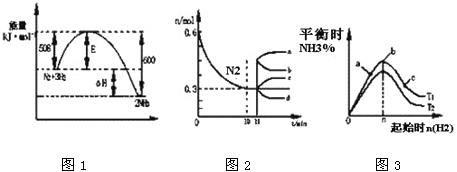
下列说法正确的是
A. 该反应为自发反应,由图1可得加入适当的催化剂,E和△H都减小
B. 图2中0~10min内该反应的平均速率v(H2)=0.045mol·L-1·min-1,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为d
C. 图3中a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点
D. 图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则:T1>T2,K1>K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关化学反应的说法,正确的是
A. 自发反应都是放热反应B. 自发反应都是熵增大的反应
C. 自发反应一定能实现D. 非自发反应在一定条件下能实现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烧瓶中放入铜片和稀硝酸,来制取较纯净的一氧化氮,反应开始后发现烧瓶中充满红棕色气体,这时的操作应是 ( )。
A. 立即接上收集容器,用向上排空气法收集
B. 待烧瓶中红棕色气体消失后,用向上排空气法收集
C. 待烧瓶中红棕色气体消失后,用排水法收集
D. 立即用排水法收集
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向2L恒容密闭容器中充入1mol PCl5 , 发生反应:PCl5(g)PCl3(g)+Cl2(g) 反应过程中测定的部分数据见表(反应过程中条件不变):
t/s | 0 | 30 | 150 | 250 | 350 | 450 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 | x |
请回答下列问题:
(1)x 的值是;
(2)0﹣50s 内,用PCl3的浓度变化表示的化学反应速率是;
(3)250s 以后,Cl2的物质的量不再改变的原因是;
(4)250s 时,容器中Cl2的物质的量是 , PCl5的物质的量是 , PCl5的转化率是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由反应物X转化为Y和Z的能量变化如图所示。下列说法不正确的是( )

A. 方程式2X=3Y △H=E3-E2 B. X、Y、Z的能量从大到小为Y>X>Z
C. 降低压强有利于提高Y的产率 D. 降低温度有利于提高Z的产率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于可再生能源的是( )
①天然气 ②生物质能 ③地热能 ④石油 ⑤太阳能 ⑥潮汐能 ⑦风能 ⑧氢能
A.①②③④B.②③⑤⑥⑦⑧C.④⑤⑥⑦⑧D.①②③⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,硝酸越稀,还原产物中氮元素的化合价越低.某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出.在反应结束后的溶液中,逐滴加入4mol/L NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.下列说法不正确的是( ) 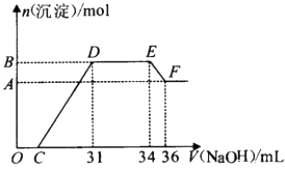
A.OC段离子反应方程式为H++OH﹣═H2O
B.溶液中n(NH ![]() )=0.012 mol
)=0.012 mol
C.溶液中结合OH﹣能力最强的离子是H+ , 最弱的离子是Al3+
D.欲测定F点沉淀的质量,实验步骤是:过滤、洗涤、干燥、称量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com