
| A. | 在熔化状态下能导电的化合物一定是离子晶体 | |
| B. | 分子晶体的状态变化只需克服分子间作用力 | |
| C. | 金属键的本质是金属离子与自由电子间的相互作用 | |
| D. | 原子晶体中只存在非极性共价键 |
分析 A.离子晶体在熔化状态下能电离出自由移动的离子;
B.只需克服分子间作用力,则晶体为分子晶体;
C.金属阳离子带正电,自由电子带负电;
D.同种元素原子之间形成非极性键,不同原子之间形成极性键.
解答 解:A.离子晶体在熔化状态下能电离出自由移动的离子,所以在熔融状态下能导电,故A正确;
B.分子晶体的状态变化,只需克服分子间作用力即可,故B正确;
C.金属阳离子带正电,自由电子带负电,则金属键是金属阳离子与自由电子间的相互作用,故C正确;
D.二氧化硅是原子晶体,晶体中存在极性键,故D错误;
故选D.
点评 本题考查化学键,为高频考点,把握化学键形成的一般规律及常见物质中的化学键为解答的关键,注重基础知识的考查,题目难度不大.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:选择题
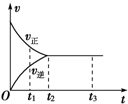
| A. | t1时,只有正方向反应 | B. | 0~t1,c(Z)在减小 | ||
| C. | t2~t3,反应不再进行 | D. | t2~t3,各物质的浓度不再发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiCl4是氧化剂 | B. | N2是还原剂 | C. | H2被还原 | D. | N2发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最高正价由低到高的顺序为:X、Z、Y、W | |
| B. | 原子半径由小到大的顺序为:X、Y、Z、W | |
| C. | 最外层电子数由少到多的顺序为:X、Z、Y、W | |
| D. | 简单氢化物的稳定性由弱到强的顺序为:Y、Z、W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气 | |
| B. | 检测时,电解质溶液中的H+向负极移动 | |
| C. | 正极上发生的反应为O2+4e-+2H2O═4OH- | |
| D. | 电池反应的化学方程式为CH3CH2OH+O2═CH3COOH+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | A | B | C | D | E | F | G | H |
| 原子半径(nm) | 0.130 | 0.118 | 0.090 | 0.102 | 0.073 | 0.154 | 0.037 | 0.099 |
| 主要化合价 | +2 | +3 | +2 | +6,-2 | -2 | +1 | +1 | +7,-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种不同元素的原子中,137Cs比131I多6个中子 | |
| B. | 多电子原子中,在离核较远的区域内运动的电子能量较低 | |
| C. | 同主族元素的简单阴离子还原性越强,其氢化物的稳定性越强 | |
| D. | 短周期元素X和Y的原子序数相差2,则X与Y可能同周期,也可能同主族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 方法 | 试剂 | |
| A | CO2(SO2) | 洗气 | 氢氧化钠溶液 |
| B | 氯化亚铁溶液(氯化铁) | 过滤 | 铁粉 |
| C | 水(溴) | 萃取、分液 | 酒精 |
| D | 硫酸钠(氯化铵) | 加热 | 氢氧化钠 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com