
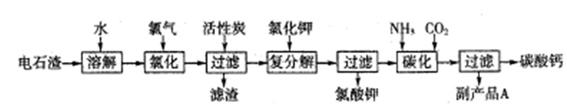
�Ե�ʯ��(��Ҫ�ɷ���Ca(OH)2����SiO2�Լ�������������)Ϊԭ�������������������̼��Ƶ��������£�
�ش��������⣺
32����ʯ������ˮ�γɵ�ʯ����ʱ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ��
33���Ȼ����̵��¶ȿ�����75��80�棬�ù�����Ҫ��Ӧ�����ӷ���ʽΪ�� _______________________________________________________________
34���������м������̿��������
35��̼�������У�������Һ��ͨ�백������ͨ��CO2��
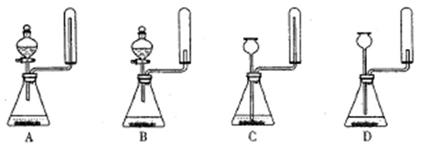
��ʵ����ͨ�����ü����Ȼ�狀��������ƻ����ķ�����ȡ������ijѧϰС��ѡȡ��ͼ��������װ����ȡ���ռ������İ�����

����������������Ӹ������ӿڣ�����Ϊ��ȷ��˳��Ϊa�� �� �� �� ��i��������i����©���������� ��
��ʵ�����л����ù����������ƺ�Ũ��ˮ��ȡ�����������������ʺ���ɸ�ʵ��ļ���װ���� (����)
36������ƷA�Ļ�ѧʽΪ ��
 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д� �����ܿ����ϵ�д�
�����ܿ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и���Ӧ�У����ڼӳɷ�Ӧ����(����)
A��CH2===CH2��Br2����CH2Br��CH2Br
B��CH3CH2OH��3O22CO2��3H2O
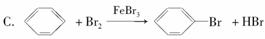
D��CH4��Cl2CH3Cl��HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ܱ����з������з�ӦaA(g) cC(g)��dD(g)����Ӧ�ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8��������������ȷ����( )
cC(g)��dD(g)����Ӧ�ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8��������������ȷ����( )
A��A��ת���ʱ�� B��ƽ��������Ӧ�����ƶ�
C��D������������ D��a �� c��d
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ڼ����������ֻ������һ���Լ���

����ˮ���� ����� �����
��������Ȼ�̼��Һ ��������Һ �� �Ȼ�����Һ �� ����������Һ
A������� B������� C������� D�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ�У��������
A. ����ͨ����������Һ�У�Cl2+H2O+Ag+��AgCl��+H++HClO
B. ������ͭ��Һ�����������壺Cu2+ + S2- �� CuS��
C. ����������Һ��ͨ������������̼ ClO-+ H2O + CO2 �� HCO3-+ HClO
D. ��NaHCO3��Һ�м���������Ba(OH)2��Һ��Ba2++2HCO3-+2OH���� BaCO3��+CO32-+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�� Cu (s)+2H+ (aq)��Cu2+(aq)+ H2 (g) ��H 1
2H2O2(l)��2H2O(l) + O2 (g) ��H 2
2H2 (g) + O2 (g)��2H2O(l) ��H 3
��Ӧ Cu (s)+H2O2(l)+2H+ (aq)��Cu2+(aq)+ 2H2O(l) �ġ�H��
A����H����H 1+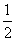 ��H 2+
��H 2+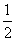 ��H 3 B����H����H 1+
��H 3 B����H����H 1+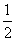 ��H 2-
��H 2-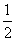 ��H 3
��H 3
C����H����H 1+2��H 2+2��H 3 D����H��2��H 1+��H 2+��H 3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Ԫ��R��T��X��Y��Z��Ԫ�����ڱ������λ�����±���ʾ�����ǵ�����������֮��Ϊ24���������ж���ȷ����
|
B������Ԫ����ԭ�Ӱ뾶������X
C����̬�⻯���ȶ��ԣ�Y��T
D��ZԪ�ص�����������Ӧ��ˮ����Ļ�ѧʽΪHZO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵�����ʾ������ȷ����
A�������ʵ������������������ֱ���ȫȼ�գ����߷ų������ࡡ
B�� ��H+��aq��+OH-��aq��===H2O��l�� ��H=-57��3kJ��mol-1��֪��������1 mol CH3COOH
��ϡ��Һ�뺬1 mol NaOH��ϡ��Һ��ϣ��ų�������С��57��3 kJ��
C����C��ʯī��== C�����ʯ�� ��H= +1��90 kJ��mol-1��֪�����ʯ��ʯī�ȶ���
D��500�桢30MPa�£���0��5mol������1��5mol ���������ܱ������г�ַ�Ӧ����
����������19��3kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g���P2NH3��g����H=-38��6kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
CCH3CH3C2H5CHCH3CH3��������ȷ����
A.2-����-3-�һ�����
B.2,3,3-��������
C.2,2-����-3-�һ�����
D.3,4,4-��������
����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com