
下列说法不正确的是( )
A.用重结晶法可以提纯苯甲酸(含砂子)、硝酸钾(含氯化钠)括号内为杂质
B.从海带中提取碘,需经过以下实验步骤:灼烧、溶解、过滤、萃取分液、蒸馏
C.加热法不可以分离I2和NH4Cl固体混合物
D.用酸性KMnO4溶液可以检验绿矾(FeSO4·7H2O)是否变质
 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源:2016-2017学年黑龙江佳木斯一中高一上月考二化学卷(解析版) 题型:选择题
下表是四个反应的有关信息:
序号 | 氧化剂 | 还原剂 | 其它反应物 | 氧化产物 | 还原产物 |
① | Cl2 | FeBr2 | FeCl3 | ||
② | KMnO4 | H2O2 | H2SO4 | O2 | MnSO4 |
③ | KClO3 | HCl(浓) | Cl2 | Cl2 | |
④ | KMnO4 | HCl(浓) | Cl2 | MnCl2 |
下列结论正确的是
A.第①组反应的氧化产物一定只有FeCl3(实为Fe3+)
B.第③组反应的产物还有KCl和H2O
C.氧化性比较:KMnO4>Cl2>Fe3+>Br2>Fe2+
D.还原性比较:H2O2>Mn2+>Cl-
查看答案和解析>>
科目:高中化学 来源:2017届福建省四地六校高三上学期12月月考化学试卷(解析版) 题型:选择题
下列有关实验的选项正确的是( )
A.下列装置中X若为苯,可用于吸收NH3或HCl,并防止倒吸 | B.加热烧杯,可以分离NaCl中NH4Cl | C.制备MgCl2晶体 | D.记录滴定终点读数为12.20 mL |
|
|
|
|
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上学期第二次月考化学试卷(解析版) 题型:推断题
四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题。
| W | X | Y | Z |
结构 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元 | 最高正价与最 |
(1)Z在元素周期表中位于 族。
(2)上述元素的最高价氧化物对应的四种水化物中,有一种物质在一定条件下均能与其它三种物质发生化学反应,该元素是 (填元素符号)。
(3)①下列可作为比较X和Y金属性强弱的依据是 (填序号)。
A.自然界中的含量 B.相应氯化物水溶液的pH
C.单质与水反应的难易程度 D.单质与酸反应时失去的电子数
②W、X、Y的离子半径由大到小的顺序为 。(填对应的离子符号)
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,反应的化学方程式是 ,混合后溶液中离子浓度由大到小的顺序是 。
(5)Y单质和Mg组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数。
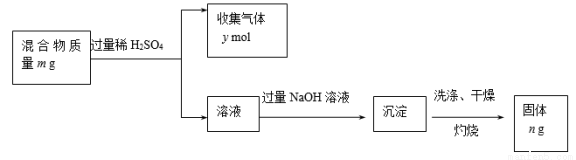
能确定混合物中Y的质量分数的数据有 (填序号)。
A.m、n B.m、y C.n、y
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上学期第二次月考化学试卷(解析版) 题型:选择题
已知A、B为单质,C为化合物。
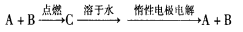
①若C溶于水后得到强碱溶液,则A可能是Na
②若C溶液遇Na2CO3,放出CO2气体,则A可能是H2
③若C溶液中滴加过量NaOH溶液,先出现浑浊后澄清,则B可能为Al
④若C溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
能实现上述转化关系的是
A.①② B.②④ C.①③ D.③④
查看答案和解析>>
科目:高中化学 来源:2016-2017陕西西安长安区一中重点班高一12月考化学卷(解析版) 题型:实验题
某铝合金中含有铁、铝、镁、铜、硅。为了测定该合金中铝的含量,现设计了如下实验:

已知:Si+2NaOH+ H2O =Na2Si O3+2
O3+2 H2↑,H2SiO3是不溶于水的弱酸。
H2↑,H2SiO3是不溶于水的弱酸。
(1)固体A的成分是:____________,溶液M中的阴离子有:____________________
(2)步骤①②③中,过滤时玻璃棒的作用是 ,步骤④中,用到的仪器有三脚架、酒精灯以及
(3)步骤③中生成沉淀的离子方程式为:____________________________
(4)在空气中将NaOH溶液滴入FeCl2溶液中,观察到的现象是 ,反应的化学方程式是
(5)该样品中铝的质 量分数是:_____________________(用a、b表示)。
量分数是:_____________________(用a、b表示)。
(6)第④步中的沉淀需用蒸馏水洗涤,若未洗涤会使测定结果___________(填偏大或偏小)。
查看答案和解析>>
科目:高中化学 来源:2016-2017陕西西安长安区一中重点班高一12月考化学卷(解析版) 题型:选择题
下列实验能达到目的的是 ( )
A.用AlCl3溶液和氢氧化钠溶液反应制备Al(OH)3
B.把饱和FeCl3溶液滴加到氢氧化钠溶液中制备Fe(OH)3 胶体
C.若Fe2O3中含少量Al2O3,先加入过量氢氧 化钠溶液,然后过滤除去
化钠溶液,然后过滤除去
D.向某溶液中先加新制氯水,再加硫氰化钾溶液,溶液变红,证明原溶液中有Fe2+
查看答案和解析>>
科目:高中化学 来源:2016-2017陕西西安长安区一中实验班高一12月考化学卷(解析版) 题型:推断题
氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将 6.00 g 甲加热至完全分解,只得到一种常见金属单质和 6.72 L 的 H2(已折算成标准状况)。甲与水反应也能放出H2,同时还产生一种白色沉淀物,该白色沉淀既可以溶于盐酸,也可溶于 NaOH 溶液。化合物乙在催化剂存在下可分解得到H2 和另一种单质气体丙,丙在标准状况下的密度为1.25 g·L-1。请回答下列问题:
(1)甲是_______________;乙是______________。( 填化学式)
(2)甲与水反应的化学方程式是____________。
(3)气体丙的分子式是____________。
(4)乙在加热条件下可与 CuO 发生反应,生成红色固体和气体丙,写出该反应的化学方程式________________。
(5)有人提出产物Cu中可能还混有Cu2O,请设计实验方案验证:__________________。
(已知:Cu2O+2H+=Cu+Cu2++H2O;Cu、Cu2O 均可以溶解在 HNO3 溶液中)
(6)甲与乙之间_____________ (填“可能”或“不可能”)发生反应产生H2,判断理由是_______________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
已知反应2CH3OH(g) CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在体积恒定的密闭容器中加入一定量的CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在体积恒定的密闭容器中加入一定量的CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度/mol·L-1 | 0.44 | 0.6 | 0.6 |
下列叙述中正确的是 ( )
A.该反应的平衡常数表达式为K=[c(CH3OCH3)×c(H2O)]/c(CH3OH)
B.此时正、逆反应速率的大小:v正<v逆
C.若经10 min后反应达到平衡,此时c(CH3OH)=0.04 mol·L-1
D.0~10min内平均反应速率v(CH3OH)=1.6 mol·(L·min)-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com