
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①②③④ |
分析 中学常见的既能与酸反应又能与碱反应的物质主要有:①两性物质:Al2O3、ZnO、Al(OH)3、Zn(OH)2、氨基酸、蛋白质等;②多元弱酸的酸式盐:NaHCO3、KHS、KHSO3、NaH2PO4等;③弱酸的铵盐及其酸式盐:(NH4)2S、NH4HS、(NH4)2CO3、NH4HCO3、CH3COONH4等;④某些具有两性的金属:Al等.
解答 解:①Al(OH)3属于两性氢氧化物,既能与酸反应生成Al3+离子,又能与碱反应生成AlO2-离子,故①正确;
②Al2O3属于两性氧化物,既能与酸反应,生成Al3+离子,又能与碱反应生成AlO2-离子,故②正确;
③(NH4)2CO3 属于弱酸的铵盐,既能与酸反应生成CO2气体,又能与碱反应生成氨气,故③正确;
④SiO2与氢氟酸反应,与其它酸不反应,故④错误,
故选A.
点评 本题考查元素化合物性质,题目难度不大,注意基础知识的积累,注意具有两性和能与酸、碱反应的区别.


科目:高中化学 来源: 题型:选择题
| A. | 反应①、②均为氧化还原反应 | |
| B. | 在反应①中金红石和焦炭均为还原剂 | |
| C. | 反应①中可燃性气体是CO | |
| D. | 反应②中有1molTi生成时,转移4mol e- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
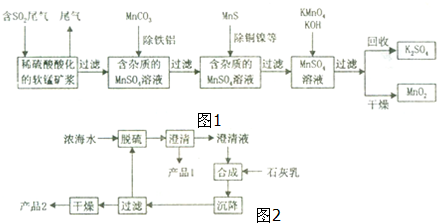
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
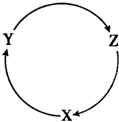 下表各组物质之间通过一步反应不能实现如图所示转化的是( )
下表各组物质之间通过一步反应不能实现如图所示转化的是( )| 选项 | X | Y | Z |
| A | SO2 | SO3 | H2SO4 |
| B | NaOH | Na2CO3 | Na2SO4 |
| C | Si | SiO2 | H2SiO3 |
| D | NO | NO2 | HNO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3使湿润的红色石蕊试纸变蓝 | |
| B. | NO气体遇空气由无色变为红棕色 | |
| C. | 向硅酸钠溶液中滴加适量的稀盐酸,有透明的凝胶形成 | |
| D. | 向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
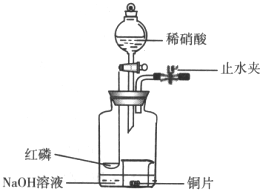 用如图示装置制备NO并验证其还原性.
用如图示装置制备NO并验证其还原性.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘水 | B. | 淀粉溶液 | C. | FeCl3溶液 | D. | 新制氢氧化铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,F元素原子的电子排布式1s22s22p63s23p5,E元素的原子结构示意图是
,F元素原子的电子排布式1s22s22p63s23p5,E元素的原子结构示意图是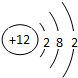
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com