
分析 碳酸钙加入过量的盐酸反应生成氯化钙、二氧化碳和水;
锌粉与稀硫酸反应生成硫酸锌和氢气;
盐酸和氢氧化钠反应生成氯化钠和水.
解答 解:碳酸钙加入过量的盐酸反应生成氯化钙、二氧化碳和水,离子方程式CaCO3+2H+=H2O+CO2↑+Ca2+;
故答案为:CaCO3+2H+=H2O+CO2↑+Ca2+;
锌粉与稀硫酸反应生成硫酸锌和氢气,离子方程式Zn+2H+=H2↑+Zn2+;
故答案为:Zn+2H+=H2↑+Zn2+;
盐酸和氢氧化钠反应生成氯化钠和水,离子方程式:H++OH-=H2O;
故答案为:H++OH-=H2O;
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
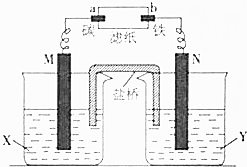 根据反应:Zn+CuSO4═Cu+ZnSO4设计原电池进行如图所示实验,滤纸上滴有酚酞和氯化钠溶液.实验进行一段时间后,在b电极附近出现红色.请回答下列问题:
根据反应:Zn+CuSO4═Cu+ZnSO4设计原电池进行如图所示实验,滤纸上滴有酚酞和氯化钠溶液.实验进行一段时间后,在b电极附近出现红色.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:100:1011 | B. | 1:12:11 | C. | 14:12:11 | D. | 14:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酚酞试液 | B. | 用石蕊溶液 | ||
| C. | NaOH溶液 | D. | 用硝酸酸化后的Ba(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状态下,1L庚烷完全燃烧后,所生成的气态产物的分子数为$\frac{7}{22.4}$NA | |
| B. | 1mol-CH3所含的电子数为10NA | |
| C. | 在人体内,180g葡萄糖完全被生理氧化所消耗的氧气的分子数为6NA | |
| D. | 0.5mol苯分子中含有1.5NA碳碳单键和1.5NA碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大于10.00mL | B. | 小于10.00mL | C. | 等于10.00mL | D. | 等于11.00mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com