
| A.溶液中的c(CH3COO-) | B.溶液中的c(H+) |
| C.溶液中的c(CH3COOH) | D.溶液中的c(OH-) |
科目:高中化学 来源:不详 题型:单选题
| A.0.5 | B.1.7 | C.10.9 | D.13.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1∶4 | B.1∶5 | C.2∶1 | D.2∶3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
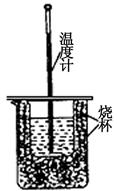
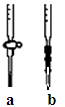
| 实验次数 | 起始滴定管读数 | 终点滴定管读数 |
| 1 | 0.00mL | 24.04mL |
| 2 | 0.50mL | 24.46mL |
| 3 | 2.50mL | 25.02mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HN3水溶液中粒子浓度大小顺序为:c(HN3)>c(H+)>c(N3-)>c(OH-) |
| B.若HN3比HCN酸性强,则相同体积相同物质的量浓度的NaN3与NaCN溶液中,离子总数NaN3比NaCN多 |
| C.NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-)>c(OH-)>c(H+) |
| D.HN3与NH3作用生成的叠氮酸铵是共价化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将水加热到100 ℃时,水的pH=6 | B.向水中滴加少量稀H2SO4 |
| C.向水中加入少量NaHCO3 | D.向水中加入少量胆矾晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
| B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净但没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
| 滴定次数 | 待测NaOH 溶液的体积来 | 0.1000mol/L盐酸的体积/mL+ | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.28 | 26.28 |
| 第二次 | 25.00 | 1.55 | 30.30 | 28.75 |
| 第三次 | 25.00 | 0.20 | 26.42 | 26.22 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com