
| A、F2 K HCl |
| B、Cl2 Al H2 |
| C、NO2 Na Br2 |
| D、O2 SO2 H2O |


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、图Ⅰ可表示对于达到平衡状态的N2(g)+3H2(g)?2NH3(g)反应,在t1时缩小容器体积,并在t2时又达到平衡 |
| B、图Ⅱ可表示体积都为1L,pH=2的盐酸和醋酸溶液分别与0.65g锌粒反应生成氢气速率的快慢 |
| C、图Ⅲ表示NO2平衡转化率与温度、压强的变化关系,由图可知:△H<0、p1<p2 |
| D、图Ⅳ可表示将等体积pH=2的盐酸和醋酸分别加水稀释过程中pH的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| A、C3N3(OH)3与HNCO为同一物质 |
| B、HNCO是一种很强的氧化剂 |
| C、1molNO2在反应中转移的电子为4mol |
| D、CO2既不是氧化产物,也不是还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯水和干木头都不导电,但木头用水浸湿后可以导电 |
| B、盛放碳酸钠溶液的试剂瓶不能用玻璃塞 |
| C、草木灰不能和铵态氮肥混合使用 |
| D、寻找高效催化剂,使水分解出产物氢气,同时释放能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4++H2O?NH3?H2O+H+ |
| B、Br-+H2O?HBr+OH- |
| C、CO32-+2H2O?H2CO3+2OH- |
| D、Fe3++3H2O?Fe(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
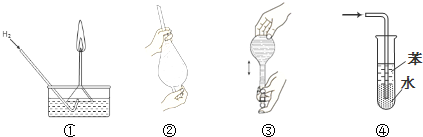
| A、操作①:使用稍浸入液面下的倒扣漏斗检验氢气的纯度 |
| B、操作②:使用CCl4萃取溴水中的溴时,振荡后需打开活塞使漏斗内气体放出 |
| C、操作③:用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否漏水 |
| D、操作④:吸收氨气或氯化氢气体并防止倒吸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com