
����Ŀ��ij��ɫ��Һ��ֻ���ܺ������������е������֣�K+��Mg2+��Fe3+��NH4+��Cl����CO32����SO42�� �� ��ÿ��ȡ100mL����ʵ�飺
�ٵ�һ�ݼ���AgNO3��Һ�г���������
�ڵڶ��ݼ�������NaOH��Һ����������û�г������������ȣ��ռ�������1.12L����״����
�۵����ݼ�������BaCl2��Һ��ø������4.30g����������������ϴ�ӣ������ʣ��2.33g��
��������ʵ�飬�϶����ڵ������� �� �϶������ڵ������� �� ����һ�����Ӳ���ȷ���Ƿ���ڣ�Ҫ�����������ӵ�ʵ����������� ��
���𰸡�NH4+��Cl����CO32����SO42����Mg2+��Fe3+��ȡ������Ʒ����ɫ��Ӧ������ɫ�ܲ����۲죬���������ɫ������K+
���������⣺�ٵ�һ�ݼ���AgNO3��Һ�г�����������ɫ����ΪAgCl��̼��������������
����ڶ�����Һ�м�������NaOH ��Һ����ȣ��ռ���1.12L����״�������壬����Ϊ�����������ʵ���Ϊ ![]() =0.05mol��ԭ��Һ��һ����0.05molNH4+��
=0.05mol��ԭ��Һ��һ����0.05molNH4+��
�����������Һ�м�������BaCl2��Һ���õ�����4.30g����������������ϴ�Ӻ�ʣ��2.33g����SO42�������ʵ���Ϊ ![]() =0.01mol����CO32�������ʵ���Ϊ
=0.01mol����CO32�������ʵ���Ϊ ![]() =0.01mol��
=0.01mol��
��Һ��һ������NH4+��Cl����CO32����SO42�����������ӹ����֪ԭ��Һ��һ��������Fe3+��Mg2+��
�ɵ���غ㣬�ܸ���ɵ����ʵ���=0.01mol��2+0.01mol��2=0.04mol��������ɵ����ʵ���=0.05mol����֪һ������Cl����
��������ӵķ���Ϊ��ȡ������Ʒ����ɫ��Ӧ������ɫ�ܲ����۲죬���������ɫ������K+��
���Դ��ǣ�NH4+��Cl����CO32����SO42����Mg2+��Fe3+��ȡ������Ʒ����ɫ��Ӧ������ɫ�ܲ����۲죬���������ɫ������K+��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����������ԼΪ1.0L�ĺ����ܱ������з�����Ӧ��2CH3OH��g���TCH3OCH3��g��+H2O��g��
����˵����ȷ���ǣ� ��
���� | �¶ȣ��棩 | ��ʼ���ʵ�����mol�� | ƽ�����ʵ�����mol�� | |
CH3OH��g�� | CH3OCH3��g�� | H2O��g�� | ||
I | 387 | 0.20 | 0.080 | 0.080 |
�� | 387 | 0.40 | ||
�� | 207 | 0.20 | 0.090 | 0.090 |
A.�÷�Ӧ������ӦΪ���ȷ�Ӧ
B.�ﵽƽ��ʱ������I�е�CH3OH����������������е�С
C.����I�з�Ӧ�ﵽƽ������ʱ����������еij�
D.����ʼʱ������I�г���CH3OH 0.1mol��CH3OCH30.15mol��H2O 0.10mol����Ӧ��������Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��YԪ����������븺�۵ľ���ֵ֮����4��YԪ����MԪ���γ����ӻ��������ˮ�е�������Ӳ�ṹ��ͬ�����ӣ��û�������(����)
A. K2SB. Na2SC. Na2OD. KCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�⻯�(LiH)�������Ӿ��壬LiH��ˮ��Ӧ���Էų�������������������ȷ����( )
A.LiH��ˮ��Һ������
B.LiH�������Ӱ뾶������Ӱ뾶��
C.LiH�������ӿ��Ա���ԭ������
D.��Ӧ���ɵ���������ͻ�ԭ�����������Ϊ��12��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йص����仯����˵����ȷ����
A. ʵ����������Ƭ��ϡ�����ϡ���ᷴӦ��ȡH2
B. ����Һ�����������������
C. �������ſ������ռ�ͭ����ϡ���ᷴӦ������NO
D. �����£�N2������O2��Ӧ��������H2��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ���Ʒ����ص������Լ���ǩ�ϵIJ������ݣ��ݴˣ�����˵����ȷ���ǣ�������
A.����������ʵ���Ũ��Ϊ9.2 molL��1
B.1 mol Zn�������ĸ����ᷴӦ����2 g����
C.����200 mL 4.6 molL��1��ϡ������ȡ������50.0 mL
D.���������������ˮ���������Һ�����ʵ���Ũ�ȴ���9.2 molL��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ũ����ķ�ӦΪ3H2S��H2SO4=4S����4H2O������˵����ȷ����( )
A. �������屻��������B. ���ᱻ��������
C. ���ᱻ��ԭ��ˮD. �������屻��ԭ��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͬ��Ba��OH��2��Һ�У��ֱ�������ʵ���Ũ����ȵ�H2SO4��NaHSO4��Һ���䵼�������������Һ����仯��������ͼ��ʾ�����з�������ȷ���ǣ� �� 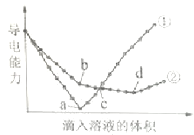
A.�ٴ����μ�H2SO4��Һ�ı仯����
B.b�㣬��Һ�д������ڵ�������Na+��OH��
C.c�㣬����Һ�к�����ͬ����OH��
D.a��d�����Ӧ����Һ��������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com