
 ,E元素在周期表中的位置是第3周期第ⅥA族,故答案为:
,E元素在周期表中的位置是第3周期第ⅥA族,故答案为: ;第3周期第ⅥA族;
;第3周期第ⅥA族; ,
, ;
;

 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、①③ |
| C、②④ | D、①②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:

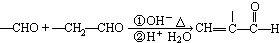

| NaCN |
| H+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1mol N2、3mol H2 | 2mol NH3 | 2mol NH3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应的平衡常数K | K甲 | K乙 | K丙 |
| 平衡时NH3的浓度/mol?L-1 | c甲 | c乙 | c丙 |
| 平衡时NH3的反应速率/mol?L-1?min-1 | v甲 | v乙 | v丙 |
| A、V甲>V丙 |
| B、K乙<K丙 |
| C、c乙>c甲 |
| D、v甲=v丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.9 g |
| B、4.6 g |
| C、5.5 g |
| D、6.9 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H6O和C4H10都有2种同分异构体 |
| B、在一定条件下,乙烯能与H2发生加成反应,苯不能与H2发生加成反应 |
| C、乙酸乙酯、乙酸均能与NaOH反应,二者分子中官能团相同 |
| D、乙醇和汽油都是可再生能源,应大力推广乙醇、汽油的使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 依据氧化还原反应2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示:
依据氧化还原反应2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com