
| 2.7g |
| 18g/mol |
| 0.8g |
| 16g/mol |


科目:高中化学 来源: 题型:
| A、1mol任何气体所占体积都约为22.4L |
| B、1molH2O在标准状况下体积为22.4L |
| C、1mol气体体积为22.4L,则一定是标准状况 |
| D、气体摩尔体积不一定是22.4L/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:

A、化学方程式中
| ||
| B、t2时N 的 v正=v逆. | ||
C、从t1到t2时刻 M的平均反应速率
| ||
| D、t3时混合气体的总物质的量不随时间的变化而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某课外活动小组利用如图1装置进行乙醇的催化氧化实验并制取乙醛(试管丁中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的镀银铜丝,约lmin后鼓入空气.请填写下列空白:
某课外活动小组利用如图1装置进行乙醇的催化氧化实验并制取乙醛(试管丁中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的镀银铜丝,约lmin后鼓入空气.请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:
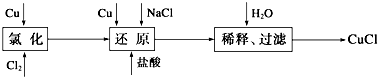
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L乙醇中含有的氧原子数为NA |
| B、标准状况下,1.12L16O2和1.12L18O2均含有0.1NA个氧原子 |
| C、在Na2O2与水的反应中,生成lmolO2转移的电子数为 4×6.02×1023 |
| D、25℃时,pH=13的Ba(OH)2溶液中含有OH-数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用新制Cu(OH)2悬浊液可鉴别麦芽糖和蔗糖. |
| B、用银镜反应可证明蔗糖是否转化为葡萄糖,但不能证明是否完全转化. |
| C、采用盐析方法,可以分离提纯蛋白质 |
| D、蔗糖溶液中滴加几滴稀H2SO4,水浴加热几分钟,加入到银氨溶液中,水浴加热有银镜产生,证明蔗糖是还原性糖. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com