
| A. | ${\;}_{55}^{133}Cs$和${\;}_{55}^{137}Cs$互为同位素 | |
| B. | ${\;}_{67}^{166}Ho$的原子核内的中子数与核外电子数之差为32 | |
| C. | 元素周期表中L层电子为奇数的元素所在族序数与该元素原子的L层电子数相等 | |
| D. | 1 mol KHSO4加热熔化可电离出2NA个阳离子 |
分析 A、质子数相同中子数不同的同种元素的不同原子互称同位素;
B、质量数=质子数+中子数计算分析;
C、L层电子为奇数的元素所在族序数与该元素原子的L层电子数相等;
D、1 mol KHSO4加热熔化可电离出NA个阳离子.
解答 解:A、${\;}_{55}^{133}Cs$和${\;}_{55}^{137}Cs$质子数相同,中子数不同,互为同位素,故A正确;
B、原子核内的中子数与核外电子数之差=166-67-67=32,故B正确;
C、L层电子为奇数,1、3、5、7,则元素所在族序数也分别是ⅠA、ⅢA、ⅤA、ⅤⅡA,故C正确;
D、1 mol KHSO4加热熔化可电离出NA个阳离子,故D错误.
故选D.
点评 本题考查了原子结构,物质性质和组成的分析,元素周期表中的有关元素知识的考查,可以根据所学知识进行回答,难度不大.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 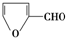 | B. |  | C. | (CH3)3CCHO | D. | CH3CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
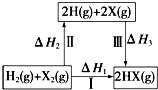
| A. | 2H(g)+2X(g)═2HX(g)△H3<0 | |
| B. | 生成HX的反应热与途径无关,所以△H1=△H2+△H3 | |
| C. | F、Cl、Br的非金属性依次减弱,所以途径Ⅱ吸收的热量依次增多 | |
| D. | F2、Cl2分别发生反应I,同一温度下的平衡常数分别为K1、K2,则K1>K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内压强增大 | B. | KO2的量保持不变 | C. | 平衡常数减小 | D. | 氧气浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数是99 | B. | 质量数是43 | C. | 中子数是99 | D. | 电子数是43 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③⑤ | C. | ①②④⑤ | D. | ②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
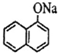 ,试剂b中官能团的名称是氯原子、碳碳双键.③的反应类型是氧化反应.
,试剂b中官能团的名称是氯原子、碳碳双键.③的反应类型是氧化反应. ;由F生成一硝化产物的化学方程式为
;由F生成一硝化产物的化学方程式为 +HNO3(浓)$→_{△}^{浓硫酸}$
+HNO3(浓)$→_{△}^{浓硫酸}$ +H2O.
+H2O.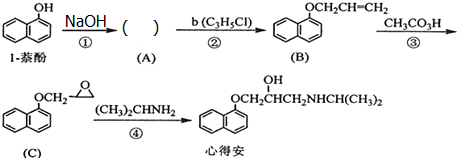
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com