
| A. | 糖类、油脂和蛋白质在一定条件下一定都能水解 | |
| B. | 除去乙醇中的乙酸用分液的方法 | |
| C. | C5H10O2能与NaHCO3反应的结构有4种 | |
| D. | C8H10的同分异构体有三种,它们的性质相似 |
分析 A.糖类中的单糖不能水解;
B.乙醇和乙酸混溶;
C.C5H10O2能与NaHCO3反应,应具有C4H9-COOH的结构特点,同分异构体取决于C4H9-;
D.C8H10如为芳香烃,满足CnH2n-6的通式,即有可能为苯的同系物,取代基可以是2个甲基或1个乙基.
解答 解:A.糖类中的单糖不能水解,如葡萄糖,故A错误;
B.乙醇和乙酸混溶,不能用分液的方法分离,应蒸馏,故B错误;
C.C5H10O2能与NaHCO3反应,应具有C4H9-COOH的结构特点,同分异构体取决于C4H9-,C4H9-的同分异构体有4种,故C正确;
D.C8H10如为芳香烃,满足CnH2n-6的通式,即有可能为苯的同系物,取代基可以是2个甲基或1个乙基,可为 等,故D错误.
等,故D错误.
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,本题注意同分异构体的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
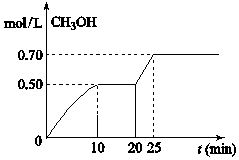 在容积固定为2L的密闭容器中,充入2molCO2和6molH2,在温度500℃时发生反应,CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,CH3OH的浓度随时间变化如右图,下列说法正确的是( )
在容积固定为2L的密闭容器中,充入2molCO2和6molH2,在温度500℃时发生反应,CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,CH3OH的浓度随时间变化如右图,下列说法正确的是( )| A. | 从开始到25分钟,CO2的转化率是35% | |
| B. | 从20分钟到25分钟,可能是缩小容器体积 | |
| C. | 其它条件不变,将温度升到800℃,平衡常数增大 | |
| D. | 从反应开始到10分钟,H2的平均反应速率v(H2)=0.15mol(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
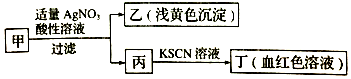
| A. | 如果甲中含有S2-,则乙是硫黄沉淀 | |
| B. | 丙中肯定含有Fe3+,所以甲是FeBr2溶液 | |
| C. | 甲中含有铁元素,可能显+2价或者+3价 | |
| D. | 若甲溶液滴加酸性KMnO4溶液,溶液变为黄色,则甲中一定含有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 发展风能、太阳能发电 | B. | 推广煤液化、气化技术 | ||
| C. | 提倡聚碳酸酯可降解塑料的使用 | D. | 普及汞锌锰干电池的使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
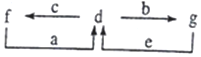 A、B、C、D为原子序数依次增大的短周期元素.已知A的某种单质是自然界中硬度最大的物质,C元素是短周期主族元素中原子半径最大的元素,a为A的最高价氧化物,b、c、d分别为B、C、D的最高价氧化物对应的水化物.化合物a~g的转化关系如图所示(部分产物己略去).下列说法错误的是( )
A、B、C、D为原子序数依次增大的短周期元素.已知A的某种单质是自然界中硬度最大的物质,C元素是短周期主族元素中原子半径最大的元素,a为A的最高价氧化物,b、c、d分别为B、C、D的最高价氧化物对应的水化物.化合物a~g的转化关系如图所示(部分产物己略去).下列说法错误的是( )| A. | 简单离子半径的大小:C>D>B | |
| B. | a中只含共价键,属于共价化合物 | |
| C. | 在水溶液中,b、g均呈酸性,c、f均呈碱性 | |
| D. | 工业上通过电解其氧化物的方法制取D的单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学习小组用下列实验方案来制备乙酸乙酯,装置(夹持装置省略)如图.
某学习小组用下列实验方案来制备乙酸乙酯,装置(夹持装置省略)如图.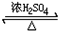 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.| 密度/(g•cm-3) | 沸点/℃ | |
| 乙酸 | 1.05 | 118.1 |
| 乙醇 | 0.780 | 78.3 |
| 乙酸乙酯 | 0.905 | 77.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖和果糖分子式均为C6H12O6,均属于还原糖 | |
| B. | 淀粉和纤维素都属于多糖,其中每个葡萄糖单元包含三个羟基 | |
| C. | 糖类并不是都有甜味,有甜味的物质也不一定是糖类 | |
| D. | 葡萄糖具有多羟基醛的结构,属于最简单的单糖 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com