
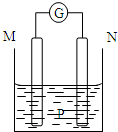
 如图所示装置中,观察到电流计指针偏转;M棒变粗,N棒变细.由此判断下表中所列M、N、P物质,其中可以成立的是( )
如图所示装置中,观察到电流计指针偏转;M棒变粗,N棒变细.由此判断下表中所列M、N、P物质,其中可以成立的是( )| M | N | P | |
| A | 锌 | 铜 | 稀硫酸溶液 |
| B | 铜 | 铁 | 稀盐酸 |
| C | 银 | 锌 | 硝酸银溶液 |
| D | 锌 | 铁 | 硝酸铁溶液 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
| A、α(A)=α(B) |
| B、α(A)>α′(A) |
| C、α(B)=α′(B) |
| D、α(A)=α′(A) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:9 | B、1:1 |
| C、1:2 | D、1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5.6 g铁与足量盐酸反应转移的电子数为0.3NA |
| B、100 mL 2.0 mol/L的盐酸与醋酸溶液中氢离子均为0.2NA |
| C、标准状况下,22.4 L氦气与22.4 L氟气所含原子数均为2 NA |
| D、20 g重水(D2O)中含有的电子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用铂电极电解氯化镁溶液:Cl-+2H2O═Cl2↑+H2↑+2OH- |
| B、氟气与水反应:F2+H2O═H++F-+HFO |
| C、NaHSO3溶液呈弱酸性是因为:HSO3-+H2O?SO32-+H3O+ |
| D、沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:FeCl3+3H2O═Fe(OH)3↓+3HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com