
某温度下,在2 L的密闭容器中,X、Y、Z三种物质随时间变化的曲线如图所示。
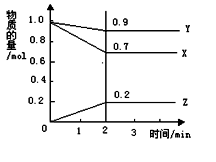
由图中数据分析:该反应的化学方程式为: 。反应开始至2 min ,Z的平均反应速率为 。
3X+Y![]() 2Z;0.05mol/(L·min)
2Z;0.05mol/(L·min)
本题考查化学反应速率的计算及化学方程式的书写,化学反应中生成物或反应物的物质的量的变化按化学方程式中的系数比进行的,这是解题的关键。同时处理图象题,要弄明白两坐标的意义及数值的确定和单位的换算等。依据图象可知,X、Y的浓度减小,说明它是反应物;Z浓度增加,说明它是生成物,且同一化学反应方程式中不同反应混合物前的化学计量数与对应的各物质所表示反应速率成正比,与对应的各物质的物质的量的改变成正比,故方程式为:3X+Y![]() 2Z;又依据图象可知,Z的物质的量增加了0.2mol,用去时间2 min,则υ(Z)=0.05mol/(L·min)。
2Z;又依据图象可知,Z的物质的量增加了0.2mol,用去时间2 min,则υ(Z)=0.05mol/(L·min)。


科目:高中化学 来源: 题型:
某温度下,在2 L的密闭容器内充入0.081 6 mol的N2O5发生反应:2N2O54NO2+O2,经过1 min后,测得c(N2O5)=0.030 mol?L-1,则该反应速率为 ( )
A.v(N2O5)=1.08×10-4 mol?(L?s)-1 B.v(NO2)=1.08×10-4 mol?(L?s)-1
C.v(O2)=9.0×10-5 mol?(L?s)-1 D.2v(NO2)=v(N2O5)
查看答案和解析>>
科目:高中化学 来源: 题型:
A.v(N2O5)=1.08×10-4 mol·(L·s)-1 B.v(NO2)=1.08×10-4 mol·(L·s)-1
C.v(O2)=9.0×10-5 mol·(L·s)-1 D.2v(NO2)=v(N2O5)
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省沧县中学高二10月月考化学试卷(带解析) 题型:填空题
(8分)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
| T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源:2014届河北省高二10月月考化学试卷(解析版) 题型:填空题
(8分)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
|
T/℃ |
700 |
800 |
830 |
1 000 |
1 200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应为________反应(填“吸热”“放热”).
(2)能判断该反应是否已达化学平衡状态的依据是________.
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O)d.c(CO2)=c(CO)
(3)某温度下,在2 L的密闭容器中,加入1 mol CO2和1 mol H2充分反应达平衡时,CO平衡浓度为0.25 mol/L,试判断此时的温度为________℃.
(4)若在(3)所处的温度下,在1 L的密闭容器中,加入2 mol CO2和3 mol H2充分反应达平衡时,H2的物质的量为________.
a.等于1.0 mol b.大于1.0 mol
c.大于0.5 mol d.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com