
下列各组中两种微粒所含电子数不相等的是( )
A.H3O+ 和OH- B.CO和N2
C.HNO2和NO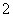 D.CH
D.CH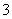 和NH
和NH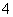
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:
已知X、Y为同周期元素,且第一电离能X<Y,下列说法中正确的是( )
A.电负性:X<Y B.周期表中,X可能在Y的右边
C.若X与Y形成化合物,则X显正价,Y显负价 D.气态氢化物的稳定性:HmY强于HnX
查看答案和解析>>
科目:高中化学 来源: 题型:
试根据下表回答问题。
某些共价键的键长数据如下所示:
| 共价键 | 键长(nm) |
| C—C | 0.154 |
| C===C | 0.134 |
| C≡C | 0.120 |
| C—O | 0.143 |
| C===O | 0.122 |
| N—N | 0.146 |
| N===N | 0.120 |
| N≡N | 0.110 |
根据表中有关数据,你能推断出影响共价键键长的因素主要有哪些?其影响的结果怎样?
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
A.以非极性键结合起来的双原子分子一定是非极性分子
B.以极性键结合起来的分子一定是极性分子
C.非极性分子只能是双原子单质分子
D.非极性分子中,一定含有非极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
已知a是H,b是N,c是O,d是S,a与其他元素形成的二元共价化合物中,分子中既含有极性共价键,又含有非极性共价键的化合物是________________________________(填化学式,写出两种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮的氢化物,则NH3分子的空间构型是________;N2H4分子中氮原子轨道的杂化类型是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X的最高价氧化物对应的水化物化学式为H2XO3,Y是地壳中含量最高的元素,则XY2由固态变为气态所需克服的微粒间作用力是________;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某催化剂中含有的活性组分为Ni、Cu和Zn的化合物,可用于二氧化碳加氢制取甲醚。甲醚是乙醇的同分异构体,其熔点为-141.5 ℃,沸点为-24.9 ℃,在加热条件下可分解成甲烷、乙烷、甲醛等。
(1)乙醇的沸点比甲醚高,其主要原因是________________________________________________________________________。
(2)甲醛分子中碳原子轨道的杂化类型为________________________________________________________________________。
(3)储氢材料化合物A是乙烷的等电子体,其相对分子质量为30.8,且A是由第二周期两种氢化物形成的化合物。加热A会缓慢释放氢气,同时A转化为化合物B,B是乙烯的等电子体。化合物A的结构式为______________(若含有配位键,要求用箭头表示),1 mol化合物B中σ键的数目是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
原子结构决定元素的性质,下列说法中正确的是( )
A.Na、Al、Cl的原子半径依次减小,Na+、Al3+、Cl-的离子半径也依次减小
B.在第ⅥA族元素的氢化物(H2R)中,热稳定性最强的一定是无毒的
C.第2周期元素原子的最外层电子数都等于其最高正化合价
D.非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com