
【题目】中科院用CO2合成了可降解塑料聚二氧化碳。下列相关说法,合理的是
A. 聚二氧化碳塑料是通过加聚反应制得的
B. 聚二氧化碳塑料与干冰互为同素异形体
C. 聚二氧化碳塑料与干冰都属于纯净物
D. 聚二氧化碳塑料的使用会产生“白色污染
科目:高中化学 来源: 题型:
【题目】已知某可逆反应:mA(g)+nB(g)![]() r C(g)在密闭容器中进行。下图表示此反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线。由曲线分析下列判断正确的是
r C(g)在密闭容器中进行。下图表示此反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线。由曲线分析下列判断正确的是

A. T1>T2,p1>p2,m+n>r,正反应吸热
B. T1<T2,p1<p2,m+n<r,正反应吸热
C. T1>T2,p1>p2,m+n<r,正反应放热
D. T1<T2,p1<p2,m+n>r,正反应放热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟氨(NH2OH)是一种还原剂。将16.00mL 0.05mol/L的羟氨酸性溶液与足量硫酸铁在煮沸条件下反应,生成的Fe2+又恰好被24.00mL 0.02mol/L的酸性KMnO4溶液所氧化。在上述反应中,羟氨的氧化产物为( )
A. NO2 B. NO C. N2O D. N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,还含有少量Fe2O3杂质。利用明矾石制备氢氧化铝的流程如下:

(1)焙烧炉中Al2(SO4)3与硫磺反应生成一种能使品红溶液褪色的物质和一种具有两性的物质,写出该反应化学方程式______________________________________________________。
(2)试剂X最好为下列试剂中的_________
A.NaOH B.CO2 C.盐酸 D.氨水
熟料溶解时,发生反应的离子方程式为_____________________________________。
(3)母液中溶质主要成分的化学式为__________。溶液调节pH后经过滤、洗涤可得Al(OH)3沉淀,证明沉淀已洗涤干净的实验操作和现象是_______________________________________________。
Ⅱ. 有100ml某透明溶液,可能含有以下离子中的若干种:Mg2+、Cu2+、Fe2+、Al3+、NH4+、K+、HCO3-、SO42-。当加入一种淡黄色粉末状固体物质时,有刺激性气味的混合气体放出,同时生成白色沉淀。当加入0.6mol淡黄色粉末时,共收集到0.8mol混合气体,且此时生成的沉淀最多。此后继续加入淡黄色粉末时,沉淀量逐渐减少,至加入0.65mol粉末后,沉淀量由0.3mol减少至0.2mol,再加入粉末后,沉淀就不再减少。由此实验现象及数据判断:
(4)淡黄色粉末为_________________;
(5)溶液中肯定有__________________离子;
(6)溶液中阳离子按量由少到多其物质的量之比为______________(H+及没有确定的离子除外)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸的工业生产可以采用生物发酵法,也可以采用有机合成法,其中的一种方法是丙酸法。
Ⅰ.生物发酵法
![]()
(1)检验淀粉是否完全水解,可以选用的一种试剂是__________(填序号)。
a.溴水 b.银氨溶液 c.碘酒 d.碘化钾淀粉溶液
(2)已知葡萄糖在乳酸菌作用下可转化为乳酸(C3H6O3)。
①写出葡萄糖与银氨溶液反应,再酸化的有机产物的结构简式:___________________。
②乳酸在Cu作催化剂时可被氧化成丙酮酸(![]() ),由以上事实推知乳酸的结构简式为_______。
),由以上事实推知乳酸的结构简式为_______。
③乳酸在一定条件下反应生成高分子化合物的化学方程式为__________________________________
④乳酸在浓H2SO4加热条件下可以生成一种能使溴水褪色的有机物A。 A在一定条件下可以合成一种常见的有机高分子化合物B,B的结构简式为____________________________。
Ⅱ.丙酸合成法

(3)反应I的反应类型是________,进行反应Ⅱ时,需要加入过量乙醇,这样做的目的是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法错误的是
A. 常温常压下,48gO2含有的氧原子数为3NA
B. 1.7g NH3含有的质子数为NA
C. 标准状况下,11.2L氦气和氢气的混合气含有的分子数为0.5NA
D. 1L 0.1 mol/LCH3CH2OH水溶液中含H原子数目为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种利用电解锰阳极泥(主要成分MnO2、MnO)制备MnO2的工艺流程如下:
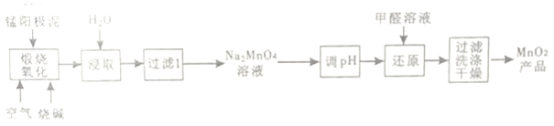
(1)“煅烧氧化”时,1mol MnO煅烧完全转化为Na2MnO4失去电子的物质的量为___________;MnO2煅烧反应的化学方程式为__________________。
(2)“浸取”时,为提高Na2MnO4的浸取率,可采取的措施有____________、____________(列举2点)
(3)“调pH”是将溶液pH 调至约为10,防止pH较低时Na2MnO4自身发生氧化还原反应,生成MnO2和___________;写出用pH试纸测定溶液pH的操作_______________。
(4)“还原”时有无机含氧酸盐生成,发生反应的化学方程式为_____________。
(5)测定产品中MnO2质量分数的步骤如下:
步骤1. 准确称取mg产品,加入c1mol·L-1Na2C2O4溶液V1mL (过量)及适量的稀硫酸,水浴加热煮沸一段时间。(已知:Na2C2O4+2H2SO4+MnO2=MnSO4+2CO2↑+2H2O+Na2SO4)
步骤2. 然后用c2mol·L-1KMnO4标准溶液滴定剩余的Na2C2O4滴定至终点时消耗KMnO4标准溶液V2mL。(已知:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+10CO2↑+K2SO4+8H2O)
步骤2达滴定终点时判断依据是_____________;产品中MnO2的质量分数为ω(MnO2)=____________(列出计算的表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,2.24L乙烷与2.24L苯含C-H键数均为0.6NA
B. 16.8gFe与足量的水蒸气加热充分反应,转移电子数为0.8NA
C. 25C时,1LpH=7的CH3COONH4溶液中含NH4+数一定为1.0×10-7NA
D. 0.2molCO2与0.1molC在密闭容器中充分反应生成CO分子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是石蜡油在炽热碎瓷片的作用下产生C2H4,并检验C2H4性质的实验,完成下列各题。

(1)B 中溶液褪色,原因是______________
(2)C 中反应的化学方程式为_____________
(3)在D 处点燃时必须进行的操作是___________,D 处反应的化学方程式为______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com