
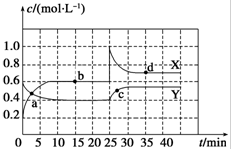
 已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g);△H>0,现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )
已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g);△H>0,现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )| A、10min前反应向△H<0的方向进行 |
| B、曲线X表示N2O4浓度随时间的变化 |
| C、第二次达到平衡时,平衡常数的值大于0.9 |
| D、反应进行至25min时,曲线发生变化的原因是加入0.4molNO2 |
| 0.62 |
| 0.4 |


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:
| A、2:3 | B、3:2 |
| C、36.5:40 | D、1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、相同体积的酸中和氢氧化钠的量相同 |
| B、相同体积的酸分别稀释成相同PH溶液,所加水的量相同 |
| C、相同体积的酸与足量锌粒反应产生氢气的量相同 |
| D、两种酸溶液中阴离子总浓度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.05 mol?L-1 |
| B、0.1 mol?L-1 |
| C、0.2mol?L-1 |
| D、0.3 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯锌与硫酸反应时,加入少量CuSO4溶液,可使反应速率加快 |
| B、甲醇和氧气以及KOH溶液构成的新型燃料电池中,其负极上发生的反应为:CH3OH+6OH-+6e-=CO2+5H2O |
| C、电解饱和食盐水制烧碱,NaOH在阳极区域产生 |
| D、用明矾净水是因为Al3+与OH-生成的Al(OH)3胶粒具有很强的吸附性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
| B、铅蓄电池放电时的负极和充电时的阳极均发生还原反应 |
| C、铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| D、镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2 晶体中阴离子和阳离子的数目之比为1:2 |
| B、同温同压下等质量的N2和CO两种气体的体积比为1:1 |
| C、同温同压下,相同体积的O2和O3两种气体中的氧原子个数比为1:1 |
| D、等质量的乙烯和环已烷所含质子数比为1:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com