
| A�� | 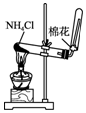 �Ʊ����� | B�� | 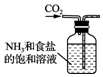 ��ȡNaHCO3 | C�� | 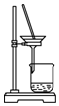 ����NaHCO3 | D�� | 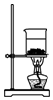 ����NaHCO3 |
���� A���Ʊ�������Ӧ���Ȼ�狀��������ƹ��壻
B��Ӧ�ӳ�����ͨ�����壻
C������������Һ�����ù��˵ķ�����
D�����չ��壬Ӧ�������н��У�
��� �⣺A���Ȼ�立ֽ����ɰ������Ȼ��⣬���¶��Ե�ʱ�������Ȼ�泥����ܵõ��������Ʊ�������Ӧ�����Ȼ�狀��������ƹ��壬��A����
B��Ӧ�ӳ�����ͨ�����壬��ֹѹǿ����B����
C������̼�����ƹ��壬���ù��˵ķ������룬��C��ȷ��
D�����չ��壬�������ձ�������ը�ѣ�Ӧ�������н��У���D����
��ѡC��
���� ���⿼���Ϊ�ۺϣ��漰������Ʊ������ʵķ����֪ʶ��Ϊ��Ƶ���㣬���ؿ���ѧ���ķ���������ʵ��������ע�����ʵ��������ԺͿ����Ե����ۣ��ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
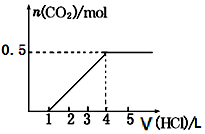 һ����CO2ͨ��ijŨ�ȵ�NaOH��Һ�У���Ӧ��õ���ҺA����A��Һ����ε���ijŨ��ϡ���ᣬ����V��HCl��������n��CO2���Ĺ�ϵ��ͼ��ʾ�������й�������ȷ���ǣ�������
һ����CO2ͨ��ijŨ�ȵ�NaOH��Һ�У���Ӧ��õ���ҺA����A��Һ����ε���ijŨ��ϡ���ᣬ����V��HCl��������n��CO2���Ĺ�ϵ��ͼ��ʾ�������й�������ȷ���ǣ�������| A�� | ͨ���CO2����Ϊ11.2 L | B�� | A��Һ��n��NaHCO3��=2n��Na2CO3�� | ||
| C�� | A��Һ�мȺ�NaOH���ֺ�Na2CO3 | D�� | A��Һ��һ��ֻ��Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
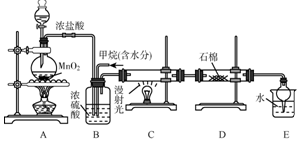 ���ü�������������ȡ����Ӧ��ȡ����Ʒ����������ڹ�ҵ���ѳ�Ϊ��ʵ��ij��ѧ��ȤС����ʵ������ģ���������̣�����Ƶ�ģ��װ����ͼ��
���ü�������������ȡ����Ӧ��ȡ����Ʒ����������ڹ�ҵ���ѳ�Ϊ��ʵ��ij��ѧ��ȤС����ʵ������ģ���������̣�����Ƶ�ģ��װ����ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��Ӧʱ��/min | n��CO��/mol | n��H2O��/mol |
| 0 | 2.00 | 3.00 |
| t1 | 0.80 | |
| t2 | 1.80 |
| A�� | ��H2��ʾ��Ӧ��t1 min�ڵ�ƽ������Ϊv��H2��=$\frac{0.60}{t_1}$mol•L-1•min-1 | |
| B�� | ���������������䣬t1ʱ�������г���3.00 mol N2���ﵽƽ��ʱ��n��CO2��=1.20 mol | |
| C�� | ���������������䣬��t2 minʱ����������ͨ��1.00 mol CO����ԭƽ����ȣ��ﵽ��ƽ��ʱCO��ת���ʽ����� | |
| D�� | �¶�����T2 K��������Ӧ��ƽ�ⳣ��Ϊ0.70��������Ӧ�ġ�H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
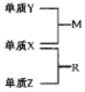 X��Y��Z�����ֶ�����Ԫ�أ�ԭ�Ӱ뾶�Ĵ�СΪ��K��Y����r��X����r��Z��������Ԫ�ص�ԭ������֮��Ϊ15��X��Y��Z����Ԫ�صij����������ʵ������¿ɷ�����ͼת����ϵ������ RΪ10���ӷ��ӣ���һ�ֳ��������ܼ�������˵���в���ȷ���ǣ�������
X��Y��Z�����ֶ�����Ԫ�أ�ԭ�Ӱ뾶�Ĵ�СΪ��K��Y����r��X����r��Z��������Ԫ�ص�ԭ������֮��Ϊ15��X��Y��Z����Ԫ�صij����������ʵ������¿ɷ�����ͼת����ϵ������ RΪ10���ӷ��ӣ���һ�ֳ��������ܼ�������˵���в���ȷ���ǣ�������| A�� | XԪ��λ�����ڱ��е�16�� | |
| B�� | X��Y��ZԪ������֮������γ�ԭ�Ӹ�����Ϊ1��1�Ļ����� | |
| C�� | X��Y��ZԪ���γɵĵ��ʾ�����ǿ��ԭ�� | |
| D�� | R�ķе����M�ķе� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3 | B�� | 4 | C�� | 5 | D�� | 6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
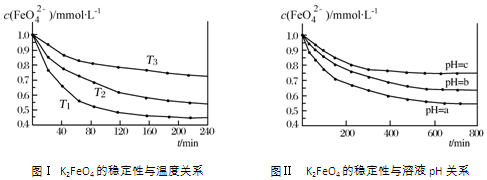
| A�� | ��ͼ���֪K2FeO4���ȶ������¶ȵ����߶����� | |
| B�� | ��ͼ���֪�¶ȣ�T1��T2��T3 | |
| C�� | ��ͼ���֪������Ӧ��H��0 | |
| D�� | ��ͼ���֪ͼ��a��c |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com