
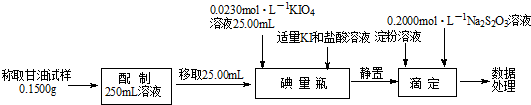
分析 Ⅰ.(1)根据电子得失守恒可知,将I2氧化为HIO4时,有关系式I2~7Cl2,根据碘的质量可计算出氯气的量;
(2)根据碘元素守恒可知,1.270g I2氧化为高碘酸时,HIO4的物质的量为$\frac{1.270g}{254g/mol}$=0.005mol,同时生成氯化氢的物质的量为0.07mol,与氢氧化钾反应的关系式为7HCl~HIO4~KOH,据此计算氢氧化钾溶液的体积;
Ⅱ.(3)碘溶液中有淀粉,所以溶液呈蓝色,用Na2S2O3标准溶液滴定达到滴定终点时溶液的蓝色会褪去,据此判断;
(4)根据题中的反应方程式可得关系式C3H8O3~$\frac{1}{2}$HIO3,I2~2Na2S2O3,3n(HIO3)+4n(HIO4)=n(I2),
碘量瓶中n(HIO3)+n(HIO4)=n(KIO4)=0.0230 mol•L×25.00mL×10-3 L•mL=5.750×10-4 mol…①
滴定时:3n(HIO3)+4n(HIO4)=n(I2)=$\frac{1}{2}$n(Na2S2O3)=$\frac{1}{2}$×0.2000 mol•L×20.00mL×10-3 L•mL-1=2.000×10-3 mol…②
根据①②可求得与C3H8O3反应的HIO3,根据HIO3的物质的量可计算出甘油的质量,进而确定样品的纯度.
解答 解:Ⅰ.(1)根据电子得失守恒可知,将I2氧化为HIO4时,有关系式I2~7Cl2,1.270g 碘的质量为$\frac{1.270g}{254g/mol}$=0.005mol,所以消耗的氯气的物质的量为0.035mol,其体积为0.035mol×22.4L/mol=0.784L,
故答案为:0.784;
(2)根据碘元素守恒可知,1.270g I2氧化为高碘酸时,HIO4的物质的量为$\frac{1.270g}{254g/mol}$×2=0.01mol,同时生成氯化氢的物质的量为0.07mol,与氢氧化钾反应的关系式为7HCl~HIO4~KOH,所以氢氧化钾溶液的体积为$\frac{0.01mol}{0.200mol•{L}^{-1}}$×8=0.05L×8=400mL,
故答案为:400;
Ⅱ.(3)碘溶液中有淀粉,所以溶液呈蓝色,所以用Na2S2O3标准溶液滴定,判断达到滴定终点的现象是滴入最后一滴标准液时,溶液蓝色刚好褪去,且保持30秒不恢复原来的颜色,
故答案为:滴入最后一滴标准液时,溶液蓝色刚好褪去,且保持30秒不恢复原来的颜色;
(4)根据题中的反应方程式可得关系式C3H8O3~$\frac{1}{2}$HIO3,I2~2Na2S2O3,3n(HIO3)+4n(HIO4)=n(I2),
碘量瓶中n(HIO3)+n(HIO4)=n(KIO4)=0.0230 mol•L×25.00mL×10-3 L•mL=5.750×10-4 mol…①
滴定时:3n(HIO3)+4n(HIO4)=n(I2)=$\frac{1}{2}$n(Na2S2O3)=$\frac{1}{2}$×0.2000 mol•L×20.00mL×10-3 L•mL-1=2.000×10-3 mol…②
①×4-②得 n(HIO3)=3.000×10-4 mol
n(C3H8O3)=$\frac{1}{2}$n(HIO3)=1.500×10-4 mol
w(C3H8O3)=$\frac{1.5×1{0}^{-4}×92×10}{0.150}$×100%=92.00%,
答:甘油样品的纯度为92.00%.
点评 本题以高碘酸钾的制备以及测定甘油的含量为载体,为高频考点,侧重于学生的分析能力、实验能力和计算能力的考查,内容涉及方程式计算、氧化还原滴定、实验基本操作等,难度中等,是对知识的综合运用和能力的考查.


科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:Na+、Fe3+、NO3-、I- | |
| B. | 水电离出的c(H+)=1×10-12mol•L-1的溶液中:K+、Al3+、Cl-、SO42- | |
| C. | c( Al 3+)=0.1 mol•L-1的溶液中:Na+、K+、HCO3-、Cl- | |
| D. | 加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 月波成露露成霜,借与南枝作淡妆 | B. | 春蚕到死丝方尽,蜡炬成灰泪始干 | ||
| C. | 粉骨碎身浑不怕,要留清白在人间 | D. | 莫道雪融便无迹,雪融成水水成冰 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 | |
| B. | 将氧气和氢气的混合气体通过灼热的氧化铜,以除去其中的氢气 | |
| C. | 用溶解、过滤的方法分离K2MnO4和MnO2固体的混合物 | |
| D. | 用分液的方法分离煤油和汽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
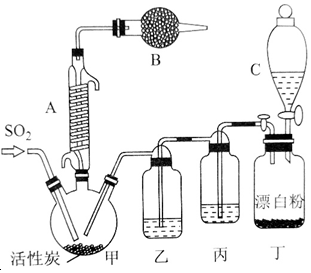 有关信息如下:硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解.回答下列问题:
有关信息如下:硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
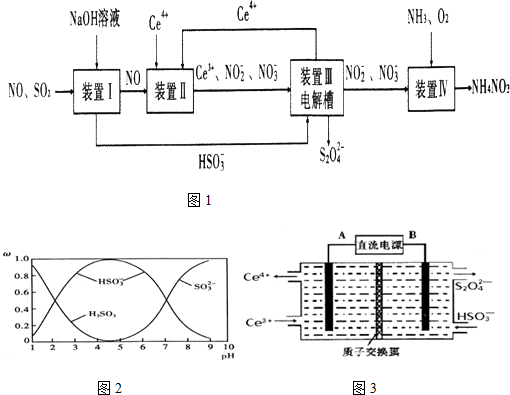
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
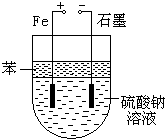 实验室用NaOH和FeSO4制取Fe(OH)2时,Fe(OH)2很容易被氧化,若采用如图所示装置制取,可以得到较纯净的Fe(OH)2.
实验室用NaOH和FeSO4制取Fe(OH)2时,Fe(OH)2很容易被氧化,若采用如图所示装置制取,可以得到较纯净的Fe(OH)2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 在稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ | |
| C. | 由C(s,石墨)=C(s,金刚石)△H=+1.90kJ/mol可知,石墨没有金刚石稳定 | |
| D. | 在101kPa时,2g的氢气完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com