
已知R2﹣的核内有x个中子,R的质量数为M,则m g R2﹣含有电子的物质的量为( )
|
| A. | (M﹣x+2)mol | B. |
| C. |
| D. |
|
| 质子数、中子数、核外电子数及其相互联系. | |
| 专题: | 原子组成与结构专题. |
| 分析: | R2﹣的核内有x个中子,R的质量数为M,则质子数为M﹣x,阴离子中,质子数+所带电荷数=核外电子数,据此计算该阴离子的核外电子数,再利用质量和质量数计算原子的物质的量,进而计算该阴离子的电子数; |
| 解答: | 解:由R2﹣的核内有x个中子,R的质量数为M,则质子数为M﹣x,故R2﹣阴离子的核外电子数为M﹣x+2,mg R2﹣的物质的量 故选D. |
| 点评: | 本题考查学生利用原子构成的简单计算,明确原子的物质的量的计算是解答本题的关键,注意电子的质量可忽略,质量数近似等于相对原子质量. |


科目:高中化学 来源: 题型:
)科学研究表明,月球上有丰富的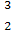 He资源,可开发利用作未来的新型能源。
He资源,可开发利用作未来的新型能源。
(1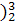 He的中子数是
He的中子数是 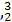 He与
He与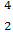 He互称为 。
He互称为 。
(2)α粒子是带有2个单位正电荷、质量数为4的原子核,由此推断α粒子含有
个质子和 个中子。
(3)在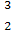 He
He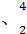 He两种核素中,原子核内的中子数之差为 ,与α粒子有相同质子数和中子数的是 。
He两种核素中,原子核内的中子数之差为 ,与α粒子有相同质子数和中子数的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
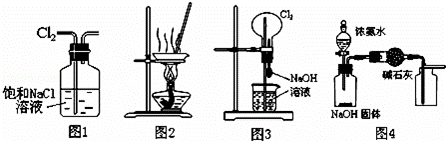
下列有关实验装置进行的相应实验,不能达到实验目的是( )
|
| A. | 用图1所示装置除去Cl2中含有的少量HCl |
|
| B. | 用图2所示装置蒸发KCl溶液制备无水KCl |
|
| C. | 用图3所示装置可以完成“喷泉”实验 |
|
| D. | 用图4所示装置制取、收集干燥纯净的NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
燃料电池的设计原理是基于将燃料燃烧时的化学能转变为电能,所以凡是燃料的燃烧反应从原理上说都可以设计成原电池反应,下列说法正确的是( )
|
| A. | 燃料电池工作时O2在正极上发生氧化反应 |
|
| B. | 燃料电池工作时O2在负极上发生氧化反应 |
|
| C. | 燃料电池工作时燃料在负极上发生还原反应 |
|
| D. | 燃料电池若以KOH溶液为介质,则工作时不会产生CO2气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的( )
|
| A. | 化学反应速率大小的决定因素是反应物的性质 |
|
| B. | 所有化学反应,温度升高其反应速率一定增大 |
|
| C. | 钢铁腐蚀、熟料老化、食物腐败等都是化学变化,减小这些反应的速率有利于生产、生活及可持续发展 |
|
| D. | 硫酸工业、硝酸工业、铁的冶炼等都涉及到化学反应且都会产生污染,减小这些反应的速率有利于降低对环境的污染也有利于国民经济的可持续发展 |
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z和W代表原子序数依次增大的四种短周期主族元素,它们满足以下条件:①元素周期表中,Z与Y相邻,Z与W也相邻;②Y、Z和W三种元素的原子最外层电子数之和为17.请填空(用元素符号或化学用语):
(1)Y是 ,Z是 ,W是 ;
(2)Y元素的最高价氧化物的化学式是 ,其对应的水化物分子式是 ;
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1.该化合物的化学式 4,其中存在的化学键类型有 ;
(4)上述四种元素中,非金属性最强的是 ,非金属性最弱的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是在相同温度下三种酸的一些数据,下列判断正确的是
| 酸 | HX | HY | HZ | ||
| 浓度(mol/L) | 0.12 | 0.2 | 0.9 | 1 | 1 |
| 电离度 | 0.25 | 0.2 | 0.1 | 0.3 | 0.5 |
| 电离常数 | K1 | K2 | K3 | K4 | K5 |
A.在相同温度,从HX的数据可以说明:弱电解质溶液,浓度越低,电离度越大,且K1>K2>K3=0.01
B.室温时,若在NaZ溶液中加水,则c((Z-)/ [c(HZ)• c(OH-)]的比值变小,若加少量盐酸,则比值变大
C.等物质的量的NaX、NaY和NaZ的混合液,c(X-)+c(Y-)-2c(Z-)=2c(HZ)-c(HX)-c(HY),且c(Z-)<c(Y-)<c(X-)
D.在相同温度下,K5>K4>K3
查看答案和解析>>
科目:高中化学 来源: 题型:
在反应3Cl2+8NH3═6NH4Cl+N2中,被氧化的氨与未被氧化的氨的分子数之比为( )
|
| A. | 1:6 | B. | 6:1 | C. | 1:3 | D. | 3:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com