
 .
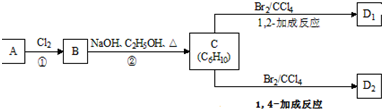
. 分析 某烃类化合物A的质谱图表明其相对分子质量为84,令组成为CxHy,则x最大值为$\frac{84}{12}$=7,红外光谱表明分子中含有碳碳双键,所以A为烯烃,所以x=6,y=12,因此A的化学式为C6H12,核磁共振氢谱表明分子中只有一种类型的氢,故A的结构简式为:(CH3)2C=C(CH3)2,A与氯气反应生成B,B为:(CH3)2C(Cl)C(Cl)(CH3)2,B在氢氧化钠、乙醇作用下加热,发生消去反应生成C,C为CH2=C(CH3)-C(CH3)=CH2,C与溴发生1,2-加成生成D1,故D1为CH2BrCBr(CH3)-C(CH3)=CH2,C与溴发生1,4-加成生成D2为CH2BrC(CH3)=C(CH3)CH2Br,据此解答.
解答 解:某烃类化合物A的质谱图表明其相对分子质量为84,令组成为CxHy,则x最大值为$\frac{84}{12}$=7,红外光谱表明分子中含有碳碳双键,所以A为烯烃,所以x=6,y=12,因此A的化学式为C6H12,核磁共振氢谱表明分子中只有一种类型的氢,故A的结构简式为:(CH3)2C=C(CH3)2,A与氯气反应生成B,B为:(CH3)2C(Cl)C(Cl)(CH3)2,B在氢氧化钠、乙醇作用下加热,发生消去反应生成C,C为CH2=C(CH3)-C(CH3)=CH2,C与溴发生1,2-加成生成D1,故D1为CH2BrCBr(CH3)-C(CH3)=CH2,C与溴发生1,4-加成生成D2为CH2BrC(CH3)=C(CH3)CH2Br,
(1)由上述分析可知,A的结构简式为:(CH3)2C=C(CH3)2,
故答案为:(CH3)2C=C(CH3)2;
(2)(CH3)2C=C(CH3)2中含有C=C双键的平面结构,4个甲基的C原子处于C=C双键的平面结构内,分子碳原子都处于同一平面,
故答案为:是;
(3)由上述分析可知,C为CH2=C(CH3)-C(CH3)=CH2,的化学名称是2,3-二甲基-1,3-丁二烯,D1为CH2BrCBr(CH3)-C(CH3)=CH2,D2为CH2BrC(CH3)=C(CH3)CH2Br,反应②是(CH3)2C(Cl)C(Cl)(CH3)2在氢氧化钠醇溶液、加热条件下发生消去反应,生成CH2=C(CH3)-C(CH3)=CH2,该反应的化学方程式为: ,
,
故答案为:2,3-二甲基-1,3-丁二烯;CH2BrCBr(CH3)-C(CH3)=CH2;CH2BrC(CH3)=C(CH3)CH2Br; .
.
点评 本题考查有机物推断,涉及卤代烃、烯、醇等的性质以及分子式的求解、有机物的空间结构和方程式的书写等,有一定的综合性,注意二烯烃的加成反应,难度中等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
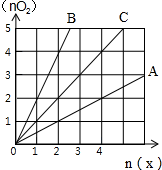
| A. | 2:1 | B. | 1:2 | C. | 1:1 | D. | 任意 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定有Al3+、Mg2+、Cl-,可能有NH4+ | |
| B. | 肯定有Al3+、Mg2+、HCO3-,肯定没有MnO4- | |
| C. | 肯定有K+、Al3+、MnO4-,可能有HCO3- | |
| D. | 肯定有Al3+、Mg2+、Cl-,可能有K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | J | K | M | N |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.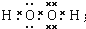 ;将乙加入浅绿色酸性溶液中,溶液变为棕黄色,写出该反应的离子方程式.
;将乙加入浅绿色酸性溶液中,溶液变为棕黄色,写出该反应的离子方程式. .与PH3相比,DC2易液化的主要原因是NH3中有氢键;
.与PH3相比,DC2易液化的主要原因是NH3中有氢键;查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子核外每层最多容纳的电子数为2n2个(n为电子层) | |
| B. | 同一原子核外的M层上的电子数一定比L层上的电子数多 | |
| C. | 如果原子只有一个电子层,该原子的质子数不超过2个 | |
| D. | 1~18号元素,每层电子数都满足2n2个电子的元素只有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | MgCl2 | Mg(OH)2 | MgCO3 |
| 溶解度(g/100g) | 74 | 0.000 84 | 0.01 |
| A. | 将表中三种物质与水混合,加热、灼烧,最终的固体产物相同 | |
| B. | 已知MgCO3的Ksp=6.82×10-6 mol2•L-2,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)•c(CO32-)=6.82×10-6 mol2•L-2 | |
| C. | 除去粗盐中含有的MgCl2杂质,最佳除杂试剂为NaOH溶液 | |
| D. | 用石灰水处理含有Mg2+和HCO3-的硬水,发生的离子反应方程式为Mg2++2HCO3-+2Ca2++4OH-═2CaCO3↓+Mg(OH)2↓+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com