
【题目】已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值减小,可以采取的措施是
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值减小,可以采取的措施是
A. 通入少量HCl气体 B. 升高温度
C. 加少量醋酸钠晶体 D. 加水
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源: 题型:
【题目】以重晶石(主要成分是BaSO4,含Al、Fe等元素的杂质)为原料制备产品(BaCl2·2H2O)的一种流程如下:
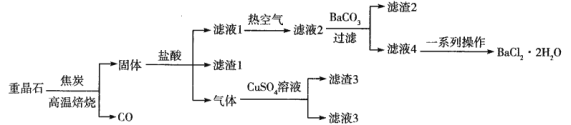
已知:滤液2主要含BaCl2,还含有AlCl3、FeCl3和HCl等杂质。298K下,Fe(OH)3、Al(OH)3完全沉淀的pH依次为3.0和5.4。
回答下列问题:
(1)高温焙烧时将重晶石粉碎的目的是______________________。若4.66 g BaSO4完全反应转移9.632×1022个电子,写出BaSO4与C反应的化学方程式:______________________。
(2)“固体”(微溶于水)与盐酸反应生成的一种气体通入CuSO4溶液中产生黑色沉淀,则生成该气体的离子方程式为______________________。滤渣3的成分是___________(填化学式)。
(3)加入BaCO3的目的是____________________________________________。
(4)常温下,Fe3+沉淀完全[溶液中c(Fe3+)=1×10-5mol·L-1]时溶液的pH=3,则Fe(OH)3的Ksp约为_____。
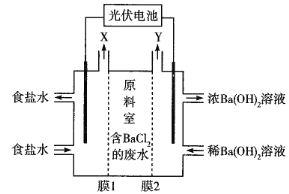
(5)滤液4经蒸发浓缩、降温结晶、过滤,洗涤和干燥,得到产品。采用电化学法以过滤后的废液为原料制备Ba(OH)2,实现资源综合利用和环境保护。气体X的电子式为____________________;写出阴极的电极反应式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)13 g C2H2(g)完全燃烧生成CO2和H2O(l)时,放出659 kJ的热量,写出表示该物质燃烧热的热化学方程式___________________________。
(2)已知反应:Cl2+2HBr===Br2+2HCl。
Ⅰ.当有0.2 mol HCl生成时放出8.1 kJ的热量。
Ⅱ.其能量变化示意图如图:

则该反应的热化学方程式为_____________________________________。由上述数据判断断开1 mol H—Cl 键与断开 1 mol H—Br键所需能量相差约为________kJ。
(3)已知:①2CO(g)+O2(g) ===2CO2(g) ΔH=-566 kJ·mol-1
②Na2O2(s)+CO2(g) ===Na2CO3(s)+1/2O2(g) ΔH=-226 kJ·mol-1
则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为________。
(4)已知CO 、H2 、CH4 的燃烧热分别为283 kJ·mol-1、286 kJ·mol-1、890 kJ·mol-1。若将a mol CH4、CO和H2的混合气体完全燃烧,生成CO2气体和液态水,且CO2和水的物质的量相等时,则放出热量(Q)的取值范围是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二铬可用作搪瓷、陶瓷、人造革、建筑材料的着色剂。由高碳铬铁合金(含Cr、Fe及C)制备三氧化二铬的工艺流程如下:
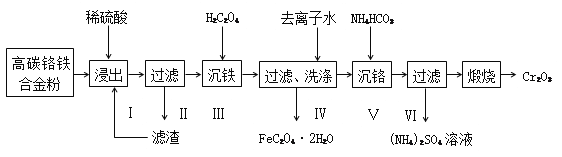
已知:Cr(OH)3是两性氢氧化物,草酸亚铁为微溶物。
回答下列问题:
(1)步骤Ⅰ浸取时,为提高浸取速率,除将高碳铬铁合金制成粉末外,还可采取的措施是__________________________(写一点);浸取铬时反应的离子方程式为_______________。
(2)步骤Ⅱ滤渣返回再次浸取的目的是_____________________________________________。
(3)步骤Ⅲ除铁时,溶液的pH对铁的去除率影响如图1所示:

图1 图2
pH小于2.3时,铁去除率低,其原因是_______________________________________。
(4)步骤Ⅳ能说明沉淀已洗涤干净的操作是________________________________________。
(5)步骤Ⅴ沉铬时,生成Cr(OH)3的化学方程式为_____________________________;沉铬时,溶液pH与铬的回收率关系如图2所示,当pH>8.5时,pH越大,铬的回收率越低,其可能原因是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,H2 + CO2![]() CO+ H2O(g)的平衡常数K=9/4。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的( )
CO+ H2O(g)的平衡常数K=9/4。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的( )

A. 平衡时,甲中和丙中H2的转化率是60%
B. 平衡时,乙中CO2的转化率小于60%
C. 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
D. 平衡时,丙中c(CO2)是甲中的2倍,是0.008mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
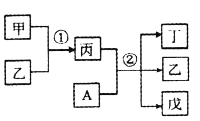
【题目】前20号元素W、X、Y、Z的原子序数依次增大,且分列四个不同周期和四个不同主族。其中A为Y元素组成的单质;甲、乙、丙、丁、戊为上述四种元素组成的二元或三元化合物;常温下乙为液体。下列说法正确的是
A. 简单离子半径:Z>Y
B. 反应①为吸热反应
C. 反应②为工业上制备漂白粉的反应原理
D. X、Y分别与Z形成的化合物中,化学键类型一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100 ℃时,向容积为2 L的密闭容器中充入一定量的X气体,发生如下反应:X(g)+2Y(g)![]() Z(g),反应过程中测定的部分数据见下表:下列说法正确的是( )
Z(g),反应过程中测定的部分数据见下表:下列说法正确的是( )
反应时间/min | n(X)/mol | n(Y)/mol |
0 | 2.00 | 2.40 |
10 | 1.00 | |
30 | 0.40 |
A. 温度为200 ℃时,上述反应平衡常数为20,则正反应为吸热反应
B. 若密闭容器体积可变,其他条件不变,在达到平衡后缩小容器体积为原来一半,则c(X)>1 mol/L
C. 保持其他条件不变,向容器中再充入1.00 mol X气体和1.20 mol Y气体,到达平衡后,X转化率增大
D. 保持其他条件不变,若再向容器中通入0.10 mol X气体,0.10 mol Y和0.10 mol Z,则v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下氢氧化锌在碱性溶液中的变化如图所示,横坐标为溶液的pH,纵坐标为Zn2+或ZnO![]() 的物质的量浓度的对数,下列说法正确的是( )
的物质的量浓度的对数,下列说法正确的是( )
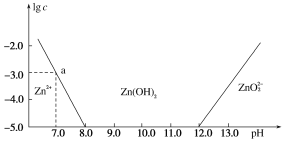
A. 依图中数据计算可得该温度下Zn(OH)2的溶度积(Ksp)=1×10-17
B. 溶液中加入足量氨水,发生反应的离子方程式为Zn2++4OH-===ZnO![]() +2H2O
+2H2O
C. 为提取工业废液中的Zn2+,可以控制溶液的pH在13左右
D. Zn2+在溶液中的存在形式与Al3+相似,碱性溶液中只以Zn(OH)2形式存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组同学在学习Cl2的实验室制法后,发现用加热浓盐酸与MnO2混合物的方法制Cl2既浪费能源又不易控制温度,他们现欲对该实验进行改进并验证Cl2的部分性质,进行了如下探究活动。
查阅资料:KMnO4和KClO3的氧化性都比MnO2强,在不加热的条件下即可与浓盐酸发生反应,从而实现制取Cl2的目的。
(1)确定反应原理:2KMnO4+16HCl(浓)===______+5Cl2↑+8H2O。
(2)选择实验装置:现有如图所示的装置,可以选择其中的____(填序号)进行实验。
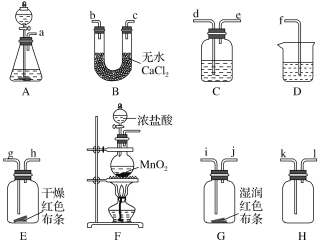
(3)装置的正确连接顺序为_______(用小写字母序号表示)。
(4)①实验时C中所装液体是________。
②在制氯气前,必须进行的一项操作是________。
③D中所装液体是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com