
科目:高中化学 来源:2015-2016学年河北省秦皇岛市卢龙县高一下学期期中考试化学试卷(解析版) 题型:填空题
把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:
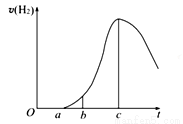
(1)曲线由O→a段不产生氢气的原因是____ ;有关反应的离子方程式为_____ ;
(2)曲线a→c段,产生氢气的速率增加较快的主要原因____ ___ ____ _ __ ;
(3)该反应若使用催化剂,能使H2产量增多吗? (填“能” 或“不能” )
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市大名等四县高二下学期期中联考化学试卷(解析版) 题型:选择题
下列实验中,所使用的装置(夹持装置略)、试剂和操作都正确的是( )
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下学期期中考试化学试卷(解析版) 题型:选择题
铜板上铁铆钉处的吸氧腐蚀原理如右图所示,下列有关说法中,不正确的是( )

A.正极电极反应式为:2H++2e—→H2↑
B.此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3
C.此过程中铜并不被腐蚀
D.此过程中电子从Fe移向Cu
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下学期期中考试化学试卷(解析版) 题型:选择题
下列反应可以设计成原电池的是( )
①CaO+H2O===Ca(OH)2 ②Fe+H2SO4===FeSO4+H2↑
③2H2O===2H2↑+O2↑ ④NaCl+AgNO3===AgCl↓+NaNO3
⑤Cu+2AgNO3===2Ag+Cu(NO3)2 ⑥Fe+2FeCl3===3FeCl2
A.①②④⑤⑥ B.②③⑤⑥ C.②⑤⑥ D.全部
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省黄石市高一下学期期中考试化学试卷(解析版) 题型:计算题
计算:将足量的铜屑加入到浓度均为2mol/L的HNO3和H2SO4的混合溶液100ml中,充分反应后,求溶液中Cu2+浓度(假设溶液体积不变)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省黄石市高一下学期期中考试化学试卷(解析版) 题型:选择题
甲、乙是周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能为( ) ①x+2 ②x+4 ③x+8 ④x+18 ⑤x+32
A.①⑤ B.② C.③ D.④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省黄石市高二下学期期中考试化学试卷(解析版) 题型:填空题
A、B、C、D、E、F分别代表原子序数依次增大的短周期元素。A和D属同族元素;B和F位于第VIIA族;A和B可形成化合物AB4;C基态原子的s轨道和p轨道的电子总数相等;E的一种单质在空气中能够自燃。 请回答下列问题:
(1)D基态原子的电子排布式是_____________________。
(2)利用价层电子对互斥理论判断EF3的立体构型是______。
(3)A所在周期元素最高价氧化物对应的水化物中,酸性最强的是______(填化学式);B和F的氢化物中沸点较高的是_____(填化学式);C、D、F的单质形成的晶体,熔点由高到低的排列顺序是_______(填化学式)。
(4)CuSO4溶液能用作E4中毒的解毒剂,反应可生成E的最高价含氧酸和铜,该反应的化学方程式是_______________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省周口市高二下学期期中考试化学试卷(解析版) 题型:填空题
乙二醇(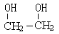 )是一种重要的化工原料,
)是一种重要的化工原料,
Ⅰ.在一定条件下以CO和H2为原料可以合成乙二醇,反应方程式如下:
2CO(g)+3H2(g) 
 (g) ΔH= a kJ/mol
(g) ΔH= a kJ/mol
(1)该反应能够自发进行,可以推出a 0;(填“>”“<”或“=”)。
(2)在一定温度下,向体积为1L的恒容密闭容器中充入2 mol CO (g)和3mol H2(g),压强为P1,达到平衡时压强变为P2,且P1:P2=15:7,则该温度下的化学平衡常数K=______
(3)只改变反应的一个条件,能使平衡体系中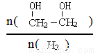 增大的措施有 (写两条)
增大的措施有 (写两条)
Ⅱ.乙二醇经连续催化氧化后可得到乙二酸(HOOC-COOH),乙二酸俗称草酸,分子式可以用H2C2O4表示,H2C2O4是一种二元弱酸,常温下其电离平衡常数K1=5.0×10-2,K2=5.0×10-5
(1)H2C2O4的电离方程式为 。
(2)Na2C2O4溶液显 (填“酸性”、“中性”或“碱性”),溶液中各离子浓度从大到小的顺序为 。
(3)已知常温下NH3·H2O的电离平衡常数K=1.75×10-5,常温下,
反应NH3·H2O + HC2O4-  NH4+ +C2O42-+H2O的平衡常数K= 。
NH4+ +C2O42-+H2O的平衡常数K= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com