
 2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£®ŅŃÖŖ1mol SO2£Øg£©Ńõ»ÆĪŖ1mol SO3£Øg£©µÄ”÷H=-99kJ•mol-1£®
2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£®ŅŃÖŖ1mol SO2£Øg£©Ńõ»ÆĪŖ1mol SO3£Øg£©µÄ”÷H=-99kJ•mol-1£®·ÖĪö £Ø1£©øł¾ŻA”¢C·Ö±š±ķŹ¾·“Ó¦Īļ×ÜÄÜĮæ”¢Éś³ÉĪļ×ÜÄÜĮ棬BĪŖ»ī»ÆÄÜ£¬»ī»ÆÄܵēóŠ”Óė·“Ó¦ČČĪŽ¹Ų£¬½ā“š£»
£Ø2£©øł¾Ż²Ī¼Ó·“Ó¦SO2µÄĪļÖŹµÄĮæÖ®±ČµČÓŚ¶ŌÓ¦µÄ”÷HÖ®±Č£»
£Ø3£©V2O5Ńõ»ÆSO2Ź±£¬×Ō¼ŗ±»»¹ŌĪŖĖļŪ·°»ÆŗĻĪļ£¬»¹Éś³ÉČżŃõ»ÆĮņ£»ĖļŪ·°»ÆŗĻĪļŌŁ±»ŃõĘųŃõ»ÆÉś³ÉV2O5£»
£Ø4£©ŅĄ¾ŻŠÅĻ¢¼ĘĖć2minŗóŃõĘųÅØ¶Č±ä»ÆĮ棬ŅĄ¾ŻV=$\frac{”÷c}{”÷t}$¼ĘĖćV£ØO2£©£¬Ķ¬Ņ»·“Ó¦ÖŠ£¬·“Ó¦ĖŁĀŹÖ®±ČµČÓŚĘä¼ĘĮæŹżÖ®±Č£¬¾Ż“Ė¼ĘĖćV£ØSO3£©£»
£Ø5£©ŅĄ¾ŻČ¼ÉÕČȵÄøÅÄīŗĶČČ»Æѧ·½³ĢŹ½£¬½įŗĻøĒĖ¹¶ØĀɼĘĖćµĆµ½£®
½ā“š ½ā£ŗ£Ø1£©ŅņĶ¼ÖŠA”¢C”¢E·Ö±š±ķŹ¾·“Ó¦Īļ×ÜÄÜĮæ”¢Éś³ÉĪļ×ÜÄÜĮ棻
¹Ź“š°øĪŖ£ŗ·“Ó¦Īļ×ÜÄÜĮæ£»Éś³ÉĪļ×ÜÄÜĮ棻
£Ø2£©Ņņ1mol SO2£Øg£©Ńõ»ÆĪŖ1mol SO3µÄ”÷H=-99kJ•mol-1£¬ĖłŅŌ2mol SO2£Øg£©Ńõ»ÆĪŖ2mol SO3µÄ”÷H=-198kJ•mol-1£¬
Ōņ2SO2£Øg£©+O2£Øg£©=2SO3£Øg£©”÷H=-198kJ•mol-1£¬
¹Ź“š°øĪŖ£ŗ-198£»
£Ø3£©V2O5Ńõ»ÆSO2Ź±£¬×Ō¼ŗ±»»¹ŌĪŖĖļŪ·°»ÆŗĻĪļ£¬»¹Éś³ÉČżŃõ»ÆĮņ£»ĖļŪ·°»ÆŗĻĪļŌŁ±»ŃõĘųŃõ»ÆÉś³ÉV2O5£¬øĆ“ß»ÆŃ»·»śĄķµÄ»Æѧ·½³ĢŹ½ĪŖSO2+V2O5ØTSO3+2VO2”¢4VO2+O2ØT2V2O5£¬
¹Ź“š°øĪŖ£ŗSO2+V2O5=SO3+2VO2£»4VO2+O2=2 V2O5 £»
£Ø4£©ŅĄ¾ŻŠÅĻ¢¼ĘĖć2minŗóŃõĘųÅØ¶Č±ä»ÆĮæ£ŗ$\frac{2mol-1.6mol}{2L}$=0.2mol/L£¬ŌņV£ØO2£©=$\frac{0.2mol/L}{2min}$=0.1mol/£ØL£®min£©£»””
Ķ¬Ņ»·“Ó¦ÖŠ£¬·“Ó¦ĖŁĀŹÖ®±ČµČÓŚĘä¼ĘĮæŹżÖ®±Č£¬¹ŹV£ØO2£©£ŗV£ØSO3£©=0.1mol/£ØL£®min£©£ŗV£ØSO3£©=1£ŗ2£»
½āµĆ£ŗV£ØSO3£©=0.2 mol/£ØL£®min£©£»
¹Ź“š°øĪŖ£ŗ0.1mol/£ØL£®min£©£»””0.2mol/£ØL£®min£©£»
£Ø5£©µ„ÖŹĮņµÄČ¼ÉÕČČĪŖ296kJ•mol-1£¬ČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ¢ŁS£Øs£©+O2£Øg£©=SO2£Øg£©”÷H1=-296 KJ•mol-1£¬ŅŃÖŖ1mol SO2£Øg£©Ńõ»ÆĪŖ1mol SO3µÄ”÷H=-99kJ•mol-1£®ČČ»Æѧ·½³ĢŹ½ĪŖ¢ŚSO2£Øg£©+$\frac{1}{2}$O2£Øg£©?SO3£Øg£©”÷H2=-99 KJ•mol-1 £»ŅĄ¾ŻøĒĖ¹¶ØĀÉ£¬¢Ś+¢ŁµĆµ½£ŗ¢ŪS£Øs£©+$\frac{3}{2}$O2£Øg£©=SO3£Øg£©”÷H=£Ø”÷H1+”÷H2£©KJ/molØT-395KJ•mol-1£»¼ĘĖćÓÉS£Øs£©Éś³É3molSO3£Øg£©¢Ū”Į3µĆµ½£ŗ3S£Øs£©+$\frac{9}{2}$O2£Øg£©=3SO3£Øg£©”÷H=3£Ø”÷H1+”÷H2£©=-1185 KJ•mol-1£¬
“š£ŗ3 S£Øs£©+$\frac{9}{2}$O2£Øg£©=3SO3£Øg£©”÷H=3£Ø”÷H1+”÷H2£©=-1185 KJ•mol-1£®
µćĘĄ ±¾ĢāĪŖ×ŪŗĻĢā£¬æ¼²éĮĖ·“Ó¦ČČµÄ¼ĘĖć”¢ČČ»Æѧ·½³ĢŹ½”¢»Æѧ·½³ĢŹ½µÄŹéŠ“£¬·“Ó¦ĖŁĀŹµÄ¼ĘĖć£¬Ć÷Č·øĒĖ¹¶ØĀɼĘĖć·“Ó¦Čȵķ½·Ø”¢ŹģĻ¤·“Ó¦ĖŁĀŹ¶ØŅå¼°¼ĘĖć·½·ØŹĒ½āĢā¹Ų¼ü£¬×¢Ņā»ī»ÆÄÜÓė·“Ó¦ČČµÄ¹ŲĻµ£¬ĢāÄæÄѶČÖŠµČ£®


 Ņ»ĻßĆūŹ¦ĢįÓÅŹŌ¾ķĻµĮŠ“š°ø
Ņ»ĻßĆūŹ¦ĢįÓÅŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | XZY3 | B£® | X3Z | C£® | XZY2 | D£® | X2ZY |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ü | B£® | ¢Ś¢Ū¢Ü | C£® | ¢Ł¢Ś¢Ū¢Ü | D£® | ¢Ł¢Ś¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe2+”¢Cl-”¢NO3-”¢Na+ | B£® | K+”¢Cu2+”¢SO42-”¢Cl- | ||
| C£® | Na+”¢K+”¢CO32-”¢SO42- | D£® | Mg2+”¢SO42-”¢OH-”¢NO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 5.1g | B£® | 10.2g | C£® | 13.6g | D£® | 15.3g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | »Æѧ·“Ó¦¼°Ąė×Ó·½³ĢŹ½ | ĘĄ¼Ū |
| A | Ńõ»ÆŃĒĢśČÜÓŚĻ”ĻõĖįFeO+2H+=Fe2++2H2O | ¼īŠŌŃõ»ÆĪļÓėĖį·“Ӧɜ³ÉŃĪŗĶĖ®£¬ÕżČ· |
| B | ĻņŃĒĮņĖį°±ČÜŅŗÖŠ¼ÓČėÉŁĮæĒāŃõ»Æ±µČÜŅŗ Ba2++SO32-=BaSO3”ż | ø“·Ö½ā·“Ó¦£¬ÓŠ³ĮµķÉś³É£¬ÕżČ· |
| C | ŗ¬n mol FeBr2µÄČÜŅŗÖŠĶØČėn mol Cl2ĶźČ«·“Ó¦2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | Ńõ»Æ»¹Ō·“Ó¦Ąė×Ó·½³ĢŹ½Āś×ćŌŖĖŲŹŲŗć”¢µē×ÓŹŲŗć”¢µēŗÉŹŲŗć£¬ÕżČ· |
| D | ČżĀČ»ÆĢśČÜŅŗµĪČėĮņĒč»Æ¼ŲČÜŅŗ£ŗFe3++3SCN-=Fe£ØSCN£©3 | ø“·Ö½ā·“Ó¦£¬ĪŽĘųĢåÉś³É£¬ĪŽ³ĮµķÉś³É£¬²»ÕżČ· |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
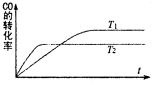 Ņ»¶ØĢõ¼žĻĀ£¬¹Ģ¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠ£¬COŗĶH2·“Ӧɜ³É¼×“¼£ŗCO£Øg£©+2H2£Øg£©?CH3OH£Øg£©£®ČēĶ¼ŹĒøĆ·“Ó¦ŌŚ²»Ķ¬ĪĀ¶ČĻĀCOµÄ×Ŗ»ÆĀŹĖꏱ¼ä±ä»ÆµÄĒśĻߣ®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
Ņ»¶ØĢõ¼žĻĀ£¬¹Ģ¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠ£¬COŗĶH2·“Ӧɜ³É¼×“¼£ŗCO£Øg£©+2H2£Øg£©?CH3OH£Øg£©£®ČēĶ¼ŹĒøĆ·“Ó¦ŌŚ²»Ķ¬ĪĀ¶ČĻĀCOµÄ×Ŗ»ÆĀŹĖꏱ¼ä±ä»ÆµÄĒśĻߣ®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©| A£® | T1£¾T2£¬øĆ·“Ó¦µÄ”÷H£¾0 | |
| B£® | ¼ÓČė“߻ƼĮæÉŅŌĢįøßCOµÄ×Ŗ»ÆĀŹ | |
| C£® | T1Ź±µÄĘ½ŗā³£ŹżK1“óÓŚT2Ź±µÄĘ½ŗā³£ŹżK2 | |
| D£® | ĪĀ¶Č½µµĶ£¬CO£Øg£©+2H2£Øg£©?CH3OH£Øl£©µÄ”÷HÖµ½«±ä“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
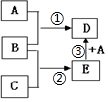 ŅŃÖŖA”¢B”¢C”¢D”¢E¾łĪŖ³£¼ūĪļÖŹ£¬ŌŚŅ»¶ØĢõ¼žĻĀĻą»„×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø·“Ó¦Ģõ¼žŗĶ²æ·Ö²śĪļŅŃŹ”ĀŌ£©£®Ēė»Ų“š£ŗ
ŅŃÖŖA”¢B”¢C”¢D”¢E¾łĪŖ³£¼ūĪļÖŹ£¬ŌŚŅ»¶ØĢõ¼žĻĀĻą»„×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø·“Ó¦Ģõ¼žŗĶ²æ·Ö²śĪļŅŃŹ”ĀŌ£©£®Ēė»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com