
聚甲基丙烯酸甲酯也是一种重要的医用高分子材料,用于人造骨、关节等。已知烯烃可被KMnO4酸性溶液氧化成二元醇,如:CH2==CH2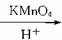 HOCH2CH2OH
HOCH2CH2OH
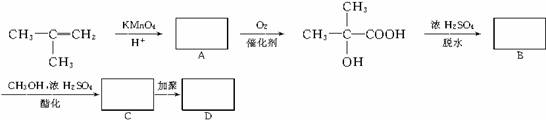
现以甲基丙烯为原料合成有机玻璃树脂,流程如下。请在下列方框中填入合适的有机物结构简式。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
阅读表中部分短周期元素的相关信息:
| 元素代号 | 相关性质 |
| T | T的单质能与冷水剧烈反应,所得的强碱性溶液中含有两种 电子数相等的阴、阳离子 |
| X | X原子的最外层电子数是其最内层电子数的3倍 |
| Y | 在第3周期元素中,Y的简单离子半径最小 |
| Z | T、X、Z组成的36电子的化合物A是家用消毒剂的主要成分 |
请回答下列问题:
(1)元素T与X按原子个数比1:1组成的化合物B所含的化学键有 (填化学键类型)。B与CO2反应的化学方程式为 。
(2)在Y与Z形成的化合物的水溶液中,逐滴加入T的最高价氧化物对应水化物的溶液直至过量(边滴加边振荡),观察到的现象是___________,写出此过程中发生反应的离子方程式 , 。
(3)已知1mol化合物A与Na2SO3在溶液中反应时转移2mol电子,写出该反应的离子方程式 。
(4)在一定条件下,X、Y两种单质以及有孔惰性电极在化合物TZ的水溶液中可形成原电池,为新型海上航标灯提供能源,写出该原电池正极的电极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
自来水可以用氯气消毒。如果实验室中临时没有蒸馏水,可以用自来水配制某些急需的药品,但有些药品若用自来水配制,则明显导致药品变质。下列哪些药品不能用自来水配制
A.FeCl2 B.NaCl C.AgNO3 D.Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列材料中属于功能高分子材料的是( )
①高分子膜 ②生物高分子材料 ③隐身材料
④液晶高分子材料 ⑤光敏高分子材料 ⑥智能高分子材料
A.①②⑤ B.②④⑤⑥ C.③④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
具有单双键交替长链(如:—CH==CH—CH==CH—CH==CH—…)的高分子有可能成为导电塑料。2000年诺贝尔(Nobel)化学奖即授予开辟此领域的3位科学家。下列高分子中可能成为导电塑料的是( )
A.聚乙烯 B.聚丁二烯 C.聚苯乙烯 D.聚乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语正确的是
A.乙醇的结构简式:C2H6O
B.CH4的比例模型:
C.工业上制取粗硅的化学方程式:SiO2+CSi+CO2↑
D.电解饱和食盐水的离子方程式:Cl-+2H2O=Cl2↑+2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,下列各组离子能大量共存的是
A.稀硫酸中:K+、Mg2+ 、AlO2-、S2O32-
B.Na2S溶液中:SO42-、K+、Cl-、Cu2+
C. =10-13mol·L-1溶液中:Fe3+、NH4+、Mg2+、 SO42-
=10-13mol·L-1溶液中:Fe3+、NH4+、Mg2+、 SO42-
D.通入大量CO2的溶液中:Na+、ClO-、CH3COO-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质的分类都正确的是(括号里的是类别)( )。
A.空气( 混合物)、C2H5OH(醇)、H2SO4(离子化合物)、CO2(非电解质) B.液氨(氢化物)、NH4Cl(铵盐)、HNO3(含氧酸)、NaOH(强电解质)
混合物)、C2H5OH(醇)、H2SO4(离子化合物)、CO2(非电解质) B.液氨(氢化物)、NH4Cl(铵盐)、HNO3(含氧酸)、NaOH(强电解质)
C.HCl(共价化合物)、CH3COOH(羧酸)、 Na2O2(碱性氧化物)、CH3I(卤代烃)
Na2O2(碱性氧化物)、CH3I(卤代烃)
D.NO2(酸性氧化物)、CH3CHO(有机物)、CO(有机物)、CH3COOCH3(酯)
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组设计用50 mL 1.0 mol/L盐酸跟50 mL 1.1 mol/L氢氧化钠溶液在如图所示装置中进行中和反应。在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过。通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:
(1) 实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是_____________________________;实验中若改用60 mL 1.0mol/L的盐酸与50 mL 1.1mol/L的氢氧化钠溶液进行反应,与上述实验相比,所放出的热量______________(填“相等”或“不相等”),若实验操作均正确,则所求中和热_________________(填“相等”或“不相等”);
| 实验 序号 | 起始温度t1/℃ | 终止温度 (t2)/℃ | 温差 (t2-t1)/℃ | ||
| 盐酸 | NaOH 溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
(2)该实验小组做了三次实验,每次取溶液各50 mL,并记录如下原始数据。已知盐酸、NaOH溶液密度近似为1.00 g/cm3,中和后混合液的比热容c=4.18×10-3 kJ/(g·℃),则该反应的中和热为ΔH= _______。
(3)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会_________(填“偏大”、“偏小”或“不变”),其原因是__________________________________。
(4)在中和热测定实验中存在用水洗涤温度计上的盐酸溶液的步骤,若无此操作步骤,则测得的中和热____________(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com