
| A. | 碳氢化合物的通式为CnH2n+2 | |
| B. | 烷烃中都有碳碳单键 | |
| C. | 烷烃分子中的碳原子只能在一条链上,不能出现支链 | |
| D. | 烷烃分子中可能出现n个甲基(n=1,2,3…) |
分析 A.饱和碳氢化合物的通式为CnH2n+2、单烯烃的通式为CnH2n;
B.甲烷不含碳碳单键;
C.烷烃分子中的碳原子可以出现支链;
D.烷烃分子中可以出现任意正整数个甲基.
解答 解:A.只含C、H元素的有机物是烃,饱和碳氢化合物的通式为CnH2n+2、单烯烃的通式为CnH2n,故A错误;
B.甲烷不含碳碳单键,除了甲烷外的所有烷烃中都含有碳碳单键,故B错误;
C.烷烃分子中的碳原子可以出现支链,也可以同一条链上,如(CH3)3CH等,故C错误;
D.烷烃中每个C原子都形成四个共价键,烷烃分子中可以出现任意正整数个甲基,如:甲烷含有一个甲基、乙烷含有两个甲基等,故D正确;
故选D.
点评 本题考查烃的有关知识,侧重考查烃的结构、通式等知识点,属于基础题,明确烃中C原子成键特点是解本题关键,注意规律中的反常现象,易错选项是BD.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| 序号 | 实验方案 | 实验现象 |
| ① | 向盛有少量溴化钠溶液的试管中滴加少量新制的氯水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈橙色 |
| ② | 向盛有少量碘化钾溶液的试管中滴加少量溴水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈紫色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2、H2和NH3的质量分数不再改变 | |
| B. | c(N2):c(H2):c(NH3)=1:3:2 | |
| C. | 单位时间里每增加1molN2,同时减少2mol NH3 | |
| D. | 单位时间里每增加1molN2,同时增加3molH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
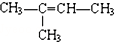
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不同金属的冶炼方法选择的原则主要是依据金属离子得电子的能力 | |
| B. | 金属的冶炼都是置换反应 | |
| C. | 应该大力开发金属矿物资源以满足人类生产生活的需要 | |
| D. | 工业上从海水中提取镁:海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{灼烧}{→}$MgO$\stackrel{电解}{→}$Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
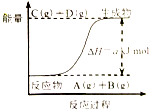
| A. | 若此反应过程中有电子转移,可设计成原电池 | |
| B. | 当A、B、C、D的浓度相同时,反应处于平衡状态 | |
| C. | 当A的消耗速率与C的消耗速率相同时处于平衡状态 | |
| D. | 该反应只有在加热条件下才能进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
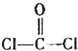 的空间结构为平面三角形.
的空间结构为平面三角形.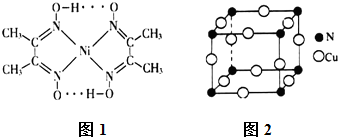
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molSiO2含有2NA个Si-O键 | |
| B. | 1molNa2O2固体中含离子总数为3NA. | |
| C. | 标准状况下,22.4 L SO3所含分子数为NA. | |
| D. | 1L0.5mol/L的MgCl2溶液中,含有Mg2+个数为0.5NA. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com