
【题目】纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B的单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能/(kJ·mol-1) | I1 | I2 | I3 | I4 |
A | 932 | 1 821 | 15 390 | 21 771 |
B | 738 | 1 451 | 7 733 | 10 540 |
(1)某同学根据上述信息,推断B的核外电子排布如下图所示,该同学所画的电子排布图违背了________。
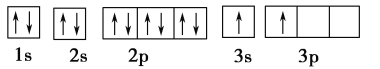
(2)ACl2分子中A原子的杂化类型为________。
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。已知金刚石中的C—C键的键长大于C60中C—C键的键长,有同学据此认为C60的熔点高于金刚石,你认为是否正确________(填“是”或“否”),并阐述理由______________________________。
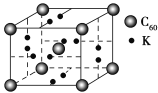
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。写出基态钾原子的价电子排布式______________,该物质的K原子和C60分子的个数比为________。
(5)继C60后,科学家又合成了Si60、N60等,C、Si、N元素的电负性由大到小的顺序是______________________________,NCl3分子的VSEPR模型为________。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则一个Si60分子中π键的数目为________。
【答案】(1)能量最低原理 (2)sp杂化 (3)否 C60为分子晶体,熔化时破坏的是分子间作用力,无需破坏共价键
(4)4s1 3∶1 (5)N>C>Si 四面体形 30
【解析】(1)E(3s)<E(3p),3s轨道排满后才能排3p轨道;(2)由表格电离能可推测出A是Be,B是Mg,BeCl2中心原子的价层电子对数为2,采取sp杂化;(3)C60是分子晶体,金刚石是原子晶体,决定二者熔沸点的作用力不同;(4)K原子序数为19,价电子为4s1,从晶胞可看出C60的个数8×![]() +1=2,K原子的个数12×
+1=2,K原子的个数12×![]() =6,K原子和C60分子的个数比为3∶1;(5)根据同周期、同主族元素原子的电负性递变规律可知:C、Si、N原子电负性由大到小的顺序是N>C>Si;NCl3中心原子价层电子对数为4,VSEPR模型为四面体;Si的价电子数为4,每个硅原子只跟相邻的3个硅原子相连且最外层都满足8电子稳定结构,所以每个Si原子周围只有1个π键,且2个Si共用1个π键,所以一个Si60分子中π键的数目为(60×1)×
=6,K原子和C60分子的个数比为3∶1;(5)根据同周期、同主族元素原子的电负性递变规律可知:C、Si、N原子电负性由大到小的顺序是N>C>Si;NCl3中心原子价层电子对数为4,VSEPR模型为四面体;Si的价电子数为4,每个硅原子只跟相邻的3个硅原子相连且最外层都满足8电子稳定结构,所以每个Si原子周围只有1个π键,且2个Si共用1个π键,所以一个Si60分子中π键的数目为(60×1)×![]() =30。
=30。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】KIO3是一种无色易溶于水的晶体,医药上可作防治地方甲状腺肿的药剂,目前碘酸钾被广泛应用于食盐加碘。一种由含碘废水制取碘酸钾的工艺如下:

(1) 检验“含碘废水”中含有的单质I2,常用的试剂是________。
(2) 进行“过滤1”时,需同时对CuI沉淀进行洗涤。在洗涤过滤滤液中可通过滴加________盐溶液来检验其是否已洗涤干净。
(3) “滤渣2”的成分为____________(填化学式)。
(4) “制KI”时,发生反应的化学方程式为____________。
(5) 江苏食用加碘盐新标准是每千克食盐中碘元素含量为25毫克(波动范围为18~33 mg/kg)。测定食盐试样中碘元素含量的步骤如下:称取4.000 g市售食盐加入锥形瓶中,依次加入适量的水、稍过量KI及稀硫酸;充分反应后,再加入12.00 mL 6.000×10-4 mol·L-1 Na2S2O3溶液,与生成的碘恰好完全反应。有关反应原理为:
KIO3+5KI+3H2SO4===3K2SO4+3I2+3H2O; I2+2S2O![]() ===2I-+S4O
===2I-+S4O![]() 。
。
①计算该食盐试样中碘元素的含量(单位mg/kg,写出计算过程)。
_______
②该食盐试样是否符合江苏食用加碘盐新标准并说明判断依据。
_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于离子反应的是( )
A.H2和O2的反应
B.铁与CuSO4溶液的反应
C.Ba(OH)2溶液和H2SO4溶液的反应
D.Zn和稀H2SO4反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常压下,下列物质按沸点升高的顺序排列正确的是 ( )。
① 辛烷 ② 十四烷 ③壬烷 ④ 丙烷
A. ②③①④ B. ④①③② C. ①②③④ D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中Cl元素全部被氧化的是
A.KClO3+6HCl=KCl+3Cl2↑+3H2O
B.2NaCl电解2Na+Cl2↑
C.H2+Cl2光照2HCl
D.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的反应,属于同一反应类型的是( )
A.由1-溴丙烷水解制1-丙醇;由乙烯与水反应制乙醇
B.由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸
C.由氯代环己烷制环己烯;由丙烯与溴制1,2-二溴丙烷
D.由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常教,下列叔述正确的是( )
A. 常温常压下,9.2gNO2气体中.分子数为0.2NA
B. pH=2的硫酸溶液中,H+数目为0.01NA
C. 将0.05molFeCl3全部转化为Fe(OH)3胶体,则胶粒数目为0.05NA
D. 20gD2O中含有的质子数为10NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com