
| A. | 标准状况下,22.4 L苯所含分子数为NA | |
| B. | 1mol甲基所含电子数为10NA | |
| C. | 常温常压下,5.6 g乙烯与丁烯的混合物中含有的氢原子数目为0.8NA | |
| D. | 12 g金刚石中含有C-C键的个数为4NA |
分析 A.标况下苯是液体;
B.甲基中性原子团,1个甲基含有9个电子;
C.乙烯和丁烯的最简式为CH2,根据最简式计算出混合物中含有氢原子数目;
D.金刚石中每个C都与令外4个C相连,则平均每个C原子成键数目为4×$\frac{1}{2}$=2个.
解答 解:A.标况下苯是液体,不能使用气体摩尔体积,故A错误;
B.1个甲基含有9个电子,1mol甲基所含电子数为9NA,故B错误;
C.乙烯和丙烯的最简式为CH2,5.6g混合气体含有0.4mol最简式CH2,含有0.8mol氢原子,含有氢原子的数目为0.8NA,故C正确;
D.金刚石中每个C都与令外4个C相连,则平均每个C原子成键数目为4×$\frac{1}{2}$=2个,12g金刚石中含C原子的物质的量为1mol,则含有C-C键的个数为2NA,故D错误;
故选:C.
点评 本题考查阿伏加德罗常数的应用,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意金刚石的结构特点.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
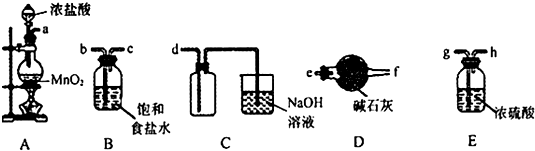
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
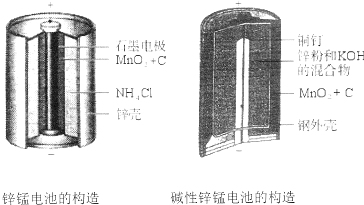
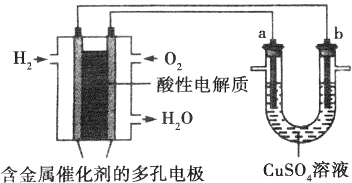
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的聚乙烯(PE)和乙烯完全燃烧消耗氧气的量相等 | |
| B. | 废弃的PE和PVC均可回收利用以减少白色污染 | |
| C. | 将PVC薄膜放入试管中加强热,产生的气体可使湿润的蓝色石蕊试纸变红 | |
| D. | PVC的单体可由PE的单体与氯化氢加成制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
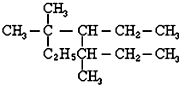 的名称是3,3,5-三甲基-4-乙基庚烷.
的名称是3,3,5-三甲基-4-乙基庚烷.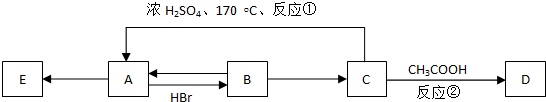
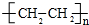 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实 验 操 作 | 结 论 |
| A | 用容量瓶配制溶液时,若定容摇匀后液面低于刻度线,补加水至与刻度线相平 | 所配溶液浓度不受影响 |
| B | 用湿润的pH试纸测定氯水的pH | 所测溶液的pH偏大 |
| C | 取少量试液于试管中,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 | 若红色石蕊试纸变蓝 则所取溶液含NH4+ |
| D | 用托盘天平称取一定质量的NaCl固体,左盘放砝码,右盘放固体 | 所称NaCl质量一定偏小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C14H30 | B. | C15H32 | C. | C16H34 | D. | C17H36 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com