
【题目】如图,向A中充入1molX、1molY,向B中充入2molX、2molY,起始时A、B的体积相等都等于aL,在相同温度和催化剂存在的条件下,关闭活塞K,使两容器中各自发生下述放热反应,X(g)+Y(g)![]() 2Z(g)+W(g);A保持恒压,B保持恒容,达平衡时,A的体积为1.4aL.下列说法错误的( )
2Z(g)+W(g);A保持恒压,B保持恒容,达平衡时,A的体积为1.4aL.下列说法错误的( )
![]()
A. 反应速率:v(B)>v(A) B. A容器中X的转化率为80%
C. 平衡时的压强:PB>2PA D. 平衡时Y体积分数:A>B
【答案】D
【解析】A选项,对于X(g)+Y(g) 2Z(g)+W(g)来说,开始时只加入反应物X和Y,该反应将向正反应方向进行,气体的总物质的量逐渐增多,直到平衡。容器A处于恒压环境下,气体物质的量增多,那么容器A的体积会随之增大,导致A中各物质的浓度减小。而容器B中,体积不变,各组分初始浓度是A容器的2倍,每个时刻的反应速率都将大于A容器,即反应速率:v(B)>v(A),故A正确;
B选项,容器A中达到平衡时,混合气体的物质的量是初始时的1.4倍。恒温恒压时,体积与气体的物质的量成正比。所以,平衡后,A容器中气体为1.4×2mol=2.8mol。即增加了0.8mol,根据化学方程式的计算可知,
X (g)+Y(g) 2Z(g)+W(g) △n
1 1
0.8mol 0.8mol
即达平衡后,反应掉0.8molX,A容器中X的转化率为80%,故B正确;
C选项,起始状态时,AB容器体积相等,B的气体物质的量是A的2倍,故起始状态时,PB=2PA。A是恒压环境,随着反应的进行A的压强不变。而容器B保持恒温恒容,是一个恒温恒容环境,随着反应的进行,B中气体的物质的量还要增大,所以B中压强越来越大,故平衡时,PB>2PA,故C正确。
D选项,起始状态时,A和B容器中Y的体积分数是相等的,容器B中的反应,是一个恒温恒容环境,随着反应的进行压强越来越大,相对于A来说,B是一个加压的过程,不利于反应向右进行,故B中Y的转化率较小,所以平衡时Y体积分数A<B,故D错误。故选D。


科目:高中化学 来源: 题型:
【题目】资源的高效利用对保护环境、促进经济持续健康发展具有重要作用,如回收利用电解精炼铜的阳极泥中含有的银、铂、金等贵重金属。提炼阳极泥的方法有多种,湿法提炼是其中重要的一种,其主要生产流程如下:
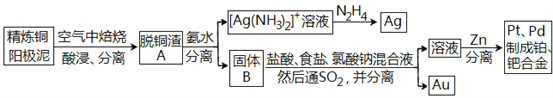
请回答下列问题:
(1)各步生产流程中都涉及了同一种分离方法,该方法需要的玻璃仪器有玻璃棒和_______。
(2)脱铜渣A中含有AgCl,它溶于浓氨水的离子方程式为________________。
(3)已知N2H4被银氨溶液氧化的产物是氮气,则每生成1molAg,需要消耗_______g N2H4。
(4)固体B中单质Au在酸性环境下与NaClO3、NaCl反应生成NaAuCl4;在NaAuCl4中Au元素的化合价为______,该反应的离子方程式为____________________。
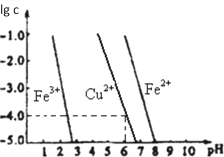
(5)阳极泥中的铜可以用FeC13溶液浸出,所得溶液主要含有的阳离子为Cu2+、Fe3+和Fe2+;结合如图分析:(其中的纵坐标代表金属阳离子浓度的对数)
①要从浸出液中提纯铜,最好先加入酸化的双氧水,目的是_______________,然后加入适量的CuO调节pH=3.7,除去______离子;
②从图中数据计算可得Cu(OH)2的Ksp约为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1993年,中国学者许志福和美国穆尔共同合成了世界上最大的碳氢分子,其中1个分子由1134个碳原子和1146个氢原子构成。关于此物质,下列说法中错误的是( )
A.是烃类化合物
B.常温下是固体
C.是高分子化合物
D.易被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向MgSO4和Al2(SO4)3的混合溶液中,逐滴加入NaOH溶液.下列图象中,能正确表示上述反应的是(横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量)( )
A.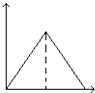
B.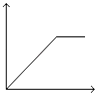
C.
D.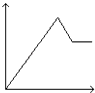
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关常温下pH均为3的醋酸和硫酸的说法正确的是( )
A. 两种溶液中,由水电离出的氢离子浓度均为1×10-11 mol·L-1
B. 分别加水稀释100倍后,两种溶液的pH仍相同
C. 醋酸中的c(CH3COO-)和硫酸中的c(SO42-)相等
D. 分别加入足量锌片,两种溶液生成H2的体积相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质间的转化在给定条件下能实现的是( )
①Al2O3 ![]() NaAlO2(aq)
NaAlO2(aq) ![]() Al(OH)3
Al(OH)3
②S ![]() SO3
SO3 ![]() H2SO4
H2SO4
③饱和NaCl(aq) ![]() NaHCO3
NaHCO3 ![]() Na2CO3
Na2CO3
④Fe2O3 ![]() FeCl3(aq)
FeCl3(aq) ![]() 无水FeCl3
无水FeCl3
⑤MgCl2(aq) ![]() Mg(OH)2
Mg(OH)2 ![]() MgO.
MgO.
A.4项
B.3项
C.2项
D.1项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在20.0 mL 0.10mol/L 氨水中滴入0.10 mol/L的盐酸。溶液的pH与所加盐酸的体积关系如图所示。已知氨水的电离度为1.32%,下列有关叙述正确的是( )
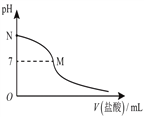
A. 该滴定过程应该选择酚酞作为指示剂
B. M点对应的盐酸体积为20.0 mL
C. M点处的溶液中![]()
D. N点处的溶液中![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com