B
分析:A.1个甲基由1个碳原子和三个氢原子构成,1个
14C中含6个质子,8个中子;
B.1mol物质的分子数为N
A,标准状况下,1mol气体的体积为22.4L;
C.pH是指溶液中氢离子浓度的负对数,pH=-lg c(H
+);
D.Cl
2溶于水中,发生的反应为:Cl
2+H
2O?HCl+HClO,该反应为可逆反应;
解答:A.17g甲基的物质的量:n=

=
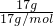
=1mol,1个
14C中含6个质子,8个中子,1个氢原子含1个质子和0个中子,1mol甲基含中子为8N
A,故A错误;
B.假设取1mol气体,在标准状况下,该气体的体积为22.4L,密度为ρg?L
-1,1mol气体的质量为22.4ρg,1mol物质的分子数为N
A,一个分子的质量为22.4ρN
Ag,故B正确;
C.25℃时,pH=13的NaOH溶液中含有氢离子浓度为PH=-lg c(H
+)=13,c(H
+)=10
-13mol/L,c(0H
-)=10
-1mol/L,1 L溶液,含有0.1N
A个氢氧根离子,故C错误;
D.Cl
2+H
2O?HCl+HClO中得到的电子为Cl
2~HCl~e-,失去的电子为Cl
2~HClO~e-,1molCl
2完全反应,转移1mol电子,0.2molCl
2转移的电子数为0.2N
A,但该反应为可逆反应,转移电子数应小于0.2N
A,故D错误;
故选B.
点评:该题涉及的重要的知识点较多,考查了可逆反应、气体摩尔体积、pH的计算、中子数与质量数间的关系,平时学习应关注这些重要的知识点,方可轻松解题.

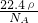 g
g =
=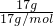 =1mol,1个14C中含6个质子,8个中子,1个氢原子含1个质子和0个中子,1mol甲基含中子为8NA,故A错误;
=1mol,1个14C中含6个质子,8个中子,1个氢原子含1个质子和0个中子,1mol甲基含中子为8NA,故A错误;

 名校课堂系列答案
名校课堂系列答案