
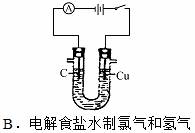
用下列实验装置进行相应实验,能达到实验目的的是



 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列叙述Ⅰ和Ⅱ均正确并有因果关系的是
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 1-己醇的沸点比己烷的沸点高 | 1-己醇和己烷可通过蒸馏初步分离 |
| B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
| C | 乙二酸可与KMnO4溶液发生反应 | 乙二酸具有酸性 |
| D | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小。请回答下列问题:
(1)FeCl3 净水的原理是 。FeCl3 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3 。
①若酸性FeCl2 废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,则该溶液的PH约为 。
②完成NaClO3 氧化FeCl2 的离子方程式:
| |
 ClO3-+
ClO3-+
|
 Fe2++
Fe2++ | |
 =
= | |
 Cl-+
Cl-+ | |
 Fe3++
Fe3++ | |
 .
. (3)FeCl3 在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
 欲使平衡正向移动可采用的方法是(填序号) 。
欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
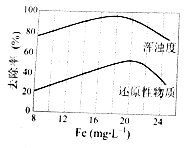
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为 mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
“ZEBRA”蓄电池的结构如图所示,电极材料多孔Ni/NiCl2和金属钠之间由钠离子导体制作的陶瓷管相隔。下列关于该电池的叙述错误的是( )
A.电池反应中有NaCl生成
B.电池的总反应是金属钠还原三价铝离子
C.正极反应为:NiCl2+2e-===Ni+2Cl-
D.钠离子通过钠离子导体在两电极间移动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于右图所示转化关系(X代表卤素)的说法错误的是
A.2H(g)+2X(g)=2HX(g) ΔH3<0
B.ΔH1=ΔH2 + ΔH3
C.Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量
按Cl、Br、I的顺序依次增多
D.途径Ⅰ生成HCl放出的热量比生成HBr的多,说明HCl
比HBr稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
在2L恒容密闭容器中投入足量M(s)和一定量的R(g),发生反应为
M(s)+R(g) X(g)+Y(g)
X(g)+Y(g) 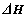 ;所得实验数据如下表所示:
;所得实验数据如下表所示:
| 实验 | 温度/℃ | 起始时R的物质的量/mol | 平衡时气体总物质的量/mol |
| ① | 300 | 2.00 | 2.80 |
| ② | 400 | 2.00 | 3.00 |
| ③ | 400 | 4.00 | a |
下列推断正确的是
A.上述反应中,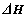 <0
<0
B.实验②中,该反应的平衡常数K=0.5
C.实验①经4 min达到平衡,0~4 min内υ(X)=0.2mol•L1•min1
D.实验③中a=6.00
查看答案和解析>>
科目:高中化学 来源: 题型:
浙江大学成功研制出能在数分钟之内将电量充满的锂电池,其成本只有传统锂电池的一半。若电解液为LiAlCl4-SOCl2,电池的总反应为:4Li+2SOCl2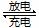 4LiCl+S+SO2。下列说法不正确的是
4LiCl+S+SO2。下列说法不正确的是
A.Li为电池的负极
B.电池的电解液可用LiCl水溶液代替
C.放电时电子从负极经外电路流向正极
D.充电时阳极反应式为:4Cl-+S+SO2-4e-=2SOCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸亚铁晶体(FeC2O4·2H2O)是一种浅黄色固体,难溶于水,受热易分解,是生产锂电池的原材料,也常用作分析试剂及显影剂等,其制备流程如下:
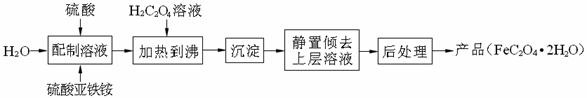
(1)配制(NH4)2Fe(SO4)2·6H2O溶液时,需加少量硫酸,目的是 。
(2)沉淀时发生反应的化学方程式为_____________________________________________________。
(3)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液的颜色由紫红色变为棕黄色,同时有气体生成。这说明草酸亚铁晶体具有_________(填“氧化”或“还原”)性。若反应中消耗1mol FeC2O4·2H2O,则参加反应的n(KMnO4)为__________。
(4)三草酸合铁酸钾晶体K3[Fe(C3O4 )3]·3H2O
(5)称取3.60g草酸亚铁晶体(摩尔质量是180g·mol-1)用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示:
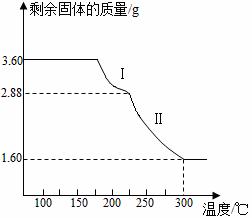
①过程Ⅰ发生反应的化学方程式为 。
②300℃时剩余固体是铁的一种氧化物,试通过计算确定该氧化物的化学式 (写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列颜色不属于因化学反应而产生的现象的是
A.无色试剂瓶中的浓硝酸呈黄色
B.久置的KI溶液呈黄色
C.新制氯水久置后变为无色
D.在普通玻璃导管口点燃纯净氢气时,火焰呈黄色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com